研究背景
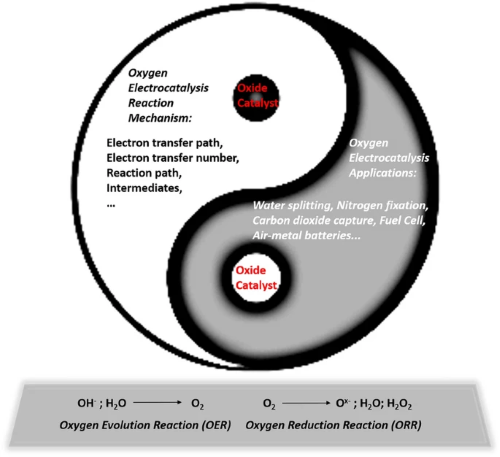
电化学氧还原反应(ORR)和析氧反应(OER)是一系列能量转换设备(如燃料电池和金属空气电池)中的基本过程。ORR和OER都具有显著的活化能垒,严重限制了利用ORR/OER的能量转换设备的整体性能。与此同时,ORR是另一个涉及氧气的非常重要的电化学反应,已经得到广泛的研究。ORR在水溶液中通过两个途径发生:从O₂到水(H₂O)的直接4电子还原或从O₂到过氧化氢(H₂O₂)的2电子还原途径。尽管贵金属电催化剂存在一定固有局限性,如低存储性,但通常用于催化OER和ORR。因此,迫切需要开发更活性和稳定的低成本电催化剂,特别是用于恶劣环境(如酸性介质)。从理论上讲,理想的氧电催化剂应能与氧物种充分结合。过渡金属氧化物被视为典型贵金属氧电催化剂的替代品。然而,用于氧还原和氧氧化反应的氧化物催化剂的开发仍面临重大挑战,如催化活性、稳定性、成本和反应机理。本综述详细讨论了设计氧化物催化剂用于氧电催化的基本原理,并提出了进一步开发氧化物催化剂面临的挑战,以及克服这些挑战的潜在策略。
Ning Han, Wei Zhang, Wei Guo, Hui Pan, Bo Jiang, Lingbao Xing,* Hao Tian,* Guoxiu Wang, Xuan Zhang,* Jan Fransaer*
本文亮点
内容简介
过渡金属氧化物被视为典型贵金属氧电催化剂的替代品。然而,用于氧还原和氧氧化反应的氧化物催化剂的开发仍面临重大挑战,如催化活性、稳定性、成本和反应机理。比利时鲁汶大学Jan Fransaer等系统的讨论了用于氧电催化的氧化物催化剂设计的基本原理,指导用于OER, ORR催化反应, 以及相关的小分子电解反应(water splitting-电解水, nitrogen fixation-氮还原, CO₂ conversion-二氧化碳还原,hydrogen peroxide generation-双氧水制备),金属空气电池,再生燃料电池等应用。最后指出了进一步开发氧化物催化剂面临的挑战,以及克服这些挑战的潜在策略。
图文导读
I 氧电催化的一般原理
析氧反应(OER)是一个涉及四个电子转移的复杂反应(图1)。传统的吸附物主导机制(AEM)通过过渡金属活性中心上的协同电子-质子转移序列进行,吸附氧中间体的结合既不能太强也不能太弱。根据AEM机制,中间体M-OH最初由氢氧根离子的一电子氧化在表面金属位点(M)上形成,作为催化活性位点。然后,通过电子转移和质子耦合步骤,M-OH转化为M-O。当氢氧根离子经历一电子氧化时,M-O转化为M-OOH,然后经过另一个电子转移和质子耦合过程产生O₂分子。与碱性介质中的OER过程相比,酸性介质中的初始步骤是H₂O在M上的吸附,随后水解离形成M-OH并释放第二个质子形成M-O。之后,另一个水分子亲核攻击M-O,最终生成M-OOH。
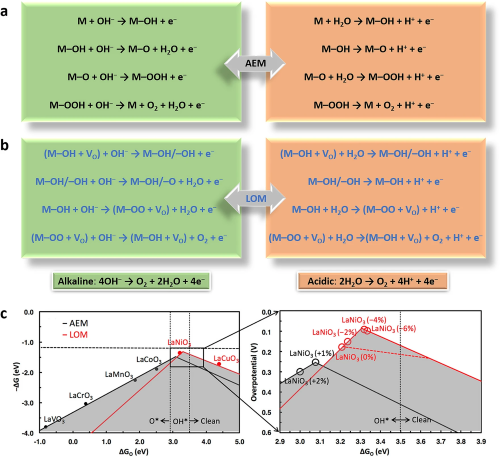
图1. 酸性和碱性介质中OER的反应路径,(a) AEM, (b) LOM, (c) 综合考虑AEM(黑色)和LOM(红色)的OER活性火山曲线。
尽管ORR在燃料电池的开发过程中得到了广泛研究,但其精确的反应机制仍在争论中。图2描绘了整体的四电子反应过程。第一个电子转移步骤涉及吸附氧物种,无论是否伴随快速的质子转移,通常被认为是贵金属(如商业上含铂)催化剂表面的RDS。最初的电子转移步骤到O₂是表面敏感的,会将H₂O从电极表面排开,并抑制HO₂⁻物种的形成。在分解成O²⁻和HO₂⁻之前,O₂是一个稳定的分子,因此可以通过反向扫描在循环伏安图中观察到。相反,过渡金属氧化物表面上的ORR反应途径与贵金属表面上的逻辑不同。为了实现氧的完全配位,过渡金属氧化物的表面阳离子与H₂O的氧相互作用。H₂O的氢原子分布在催化剂表面上,质子化通过表面阳离子(如Fe³⁺、Co³⁺、Mn⁴⁺)的还原来进行电荷补偿,从而产生OH⁻。无机化学概念有助于解释氧化物催化剂与O₂的相互作用,如晶场理论和分子轨道理论。
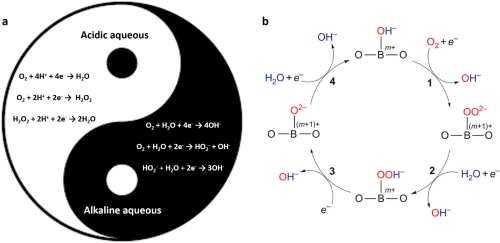
图2. (a) 酸性和碱性介质中ORR的常规反应路径;(b) 在氧化物催化剂上提出的ORR机制。
II 氧化物催化剂用于氧电催化的设计原理
开发活性、低成本的氧电催化剂对于解决效率问题至关重要。催化剂设计必须基于对OER和ORR机制以及反应过电位来源的深入理解。高性能电催化剂的开发遵循四个基本原则:丰富的电活性位点;高固有催化活性;高电导率;长期性能稳定性(图3)。基于这些原则,可以通过调控电子结构、形态、晶体结构、掺杂到晶格中的外源元素、缺陷、应变、电子轨道占据、金属-氧共价性、界面控制和工程等手段来筛选催化剂候选物。此外,控制OER/ORR的反应路径可以直接调整OER/ORR的性能,例如通过调整晶格氧阴离子的氧化还原化学平衡来平衡LOM和AEM的比例,从而促进OER过程。
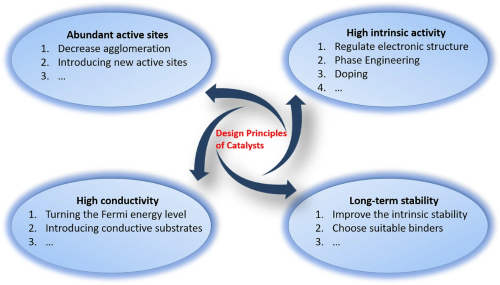
图3. OER/ORR氧化电催化剂的设计原则。
III 元素掺杂
研究人员在RuO₂中掺杂了少量的Ir(RuₓIr₁₋ₓO₂),发现在保证OER性能的同时获得了显著的稳定性增益。地球上丰富的可替换金属引入,如Co、Cu、Mn、Ni、Ce、Mg、W、Cr和Zn,是另一种提高OER活性并减少整体贵金属浓度的方法。例如,在Cu掺杂后,Cu0.3Ir0.7Oδ在酸性、中性和碱性条件下比纯IrO₂表现出增强的OER活性。研究确定,增加IrO₆和CuO₆八面体(图4)结构中的Jahn-Teller效应会增强eg和t2g轨道的提升简并性,从而提高催化性能。这通过密度泛函计算(DFT)中ΔG2和ΔG3之间的自由能差来减小理论过电位与IrO₂相比。最近,陈教授团队报道了用于酸性OER的金属有机骨架(MOF)衍生的Cr₀.₆Ru₀.₄O₂。首先,将RuCl₃负载到MIL-101(Cr)的孔隙中,然后将得到的RuCl₃-MIL-101(Cr)在450°C至600°C之间的空气中退火4小时,以产生Cr₀.₆Ru₀.₄O₂催化剂。Cr₀.₆Ru₀.₄O₂(550°C)不仅显示出优异的OER活性,而且在10,000个循环后在10 mA cm⁻²下仅有11 mV的过电位下降。DFT模拟显示了高OER性能的额外机制。在Cr5Ru3O16表面的Ru位点上,确定了RDS为1.87 eV,比RuO₂上的RDS(2.02 eV)低0.15 eV。
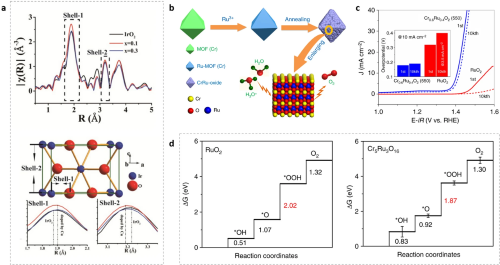
图4. (a) CuₓIr₁₋ₓOδ组分的k3归一化Ir-LIII边EXAFS傅立叶变换(上),以及IrO₂晶胞的示意图。壳层-1 Ir-O键形成,壳层-2 Ir-Ir键形成;(b) 用于酸性条件下OER的Cr₀.₆Ru₀.₄O₂电催化剂的合成示意图;(c) Cr₀.₆Ru₀.₄O₂ (550)和商业用RuO₂的第一次和第10000次循环的线性扫描伏安曲线;(d) RuO₂和Cr5Ru3O16的自由能计算图。
通过掺杂也是提高类钙钛矿氧化物OER/ORR活性和稳定性的一种通用策略。对于通用化学式为ABO₃的标准钙钛矿,其中A可以是碱土金属或稀土金属,B是过渡金属,根据掺杂策略进行了广泛的研究,用于氧电催化。在A位点、B位点甚至O位点进行掺杂,诱导氧空位,调整钙钛矿中其他部分的电子结构,可以用于修改OER/ORR活性。过渡金属的氧化态影响金属-氧杂化,因此这些钙钛矿的电子行为取决于这个参数。强电负性过渡金属表现出高的金属-氧杂化,随着电负性的增加,过渡金属氧化物的d带中心越靠近O 2p态。然而,除了金属-氧杂化外,阳离子掺杂还对八面体带来其他效应,所有这些效应在确定钙钛矿氧化物的电学特性中起重要作用。A位点通常不被视为直接参与氧电极过程的活性位点。然而,A位点阳离子可能对钙钛矿的ORR/OER性能产生间接影响。发现La1-xSrxCoO₃中的Sr取代会使八面体笼变得更加直线,原子沿Co-O-Co轴排列(图5),并增加Co阳离子的平均氧化态。结果,电导率和对OER的活性都得到显著提高。

图5. (a) 随着Sr含量的变化,Co-O-Co角度的演变;(b) 室温下La1-xSrxCoO₃的Co K边XANES光谱;(c) La1-xSrxCoO₃系列的原位电导率与电流密度(μA cm⁻²)的关系;红色圆圈代表SrCoO₂.₅;(d) SrRuO₃与掺杂钠的Sr₁₋ₓNaxRuO₃的八面体畸变对比;(e) OER火山型活性图;(f) BSCF5582和La₀.₃-5582的所有原子EXAFS光谱的径向分布函数;(g) 立方晶系基础晶粒的表面分离出六方相的LaCoO₃晶粒;(h) BSCF5582和La₀.₃-5582相比商业催化剂的ORR线性扫描伏安曲线;(i) BSCF5582和La₀.₃-5582相比商业催化剂的OER线性扫描伏安曲线。
IV eg 轨道占据
由于B位点直接参与氧气氧化还原反应,B位点的替代是调节钙钛矿催化剂的ORR/OER活性的一种直接有效的方法。Shao-Horn小组提出了一种将材料性质与催化活性联系起来的催化剂设计方法,加速了寻找高活性和廉价的过渡金属氧化物催化剂来替代贵金属催化剂(Ru、Ir、Pt)的研究。氧化物表面过渡金属阳离子的本征OER活性在eg对称性下呈现出类似火山形状的依赖性,最佳的OER活性预计在接近单位的eg占据度下发生,伴随着过渡金属氧键的强共价性(图6)。Shao-Horn小组证明了氧化物催化剂的ORR活性主要与B位点金属氧共价性相关,它作为次级活性描述符。Xu小组对尖晶石氧化物(包括MnxCO₃−xO₄、XCo/Fe₂O₄和LixMn₂O)的OER和ORR进行了进一步的描述符研究。在八面体位点上的活性阳离子的eg占据度是尖晶石的ORR/OER活性描述符,进一步确认了电子轨道填充在金属氧化物催化中的相关性。
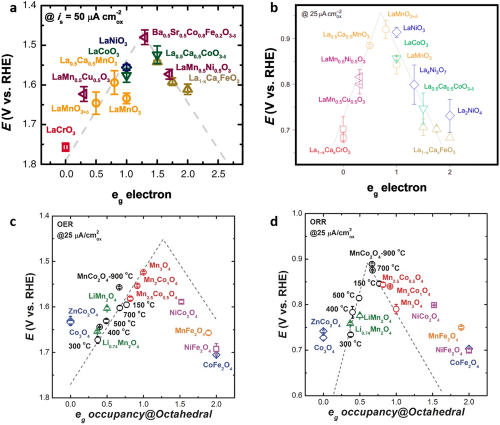
图6. (a) 钙钛矿氧化物的OER催化活性和 (b) ORR催化活性与eg对称电子的占据之间的关系;OER活性定义为50μA cm⁻²的OER电流过电位;ORR活性定义为25μA cm⁻²的ORR电流过电位;(c) 各种尖晶石氧化物的OER和(d) ORR活性,作为八面体位点活性元素的eg占据的函数。
邵教授的团队开发了SrM0.9Ti0.1O₃,其中包含不同的B位点过渡金属元素用于OER。与原始尖晶石相比,SrCo0.9Ti0.1O₃(SCT)和SrFe0.9Ti0.1O₃(SFT)均表现出增强的OER活性,并且与Ba0.5Sr0.5Co0.8Fe0.2O₃(BSCF)相当。SCT表现出比SFT更大的操作稳定性,性能超越了BSCF和IrO₂催化剂。这可以通过eg填充(1.16接近标准值1)和氧缺陷的形成来解释。Ciucci教授的团队将Nb引入到CaMnO₃(CMO)的Mn位点,并用H₂处理材料制备了CaMn0.75Nb0.25O₃−δ(H₂-CMNO),与CMO相比,H₂-CMNO表现出明显增强的OER/ORR活性。这种显著的OER/ORR活性增加可以归因于Nb⁵⁺掺杂使Mn的氧化态从+4变为+3,从而直接优化了接近单位的eg值以增加OH⁻吸附。刘教授的团队还合成了一种双钙钛矿纳米纤维PrBa0.5Sr0.5Co1.5Fe0.5O5+δ作为高效稳健的OER催化剂。Sr和Fe的共掺杂策略被证明特别成功,将固有活性提高了约5倍,这可以归因于有利的eg电子填充。水教授的团队报道了一种六方钙钛矿BaNiO₃,作为碱性介质中OER的催化剂,其活性比IrO₂高一个数量级。其潜在机制源于在OER循环过程中从BaNiO₃到BaNi0.83O₂.₅(Ba6Ni5O15)的结构转变(图7)。
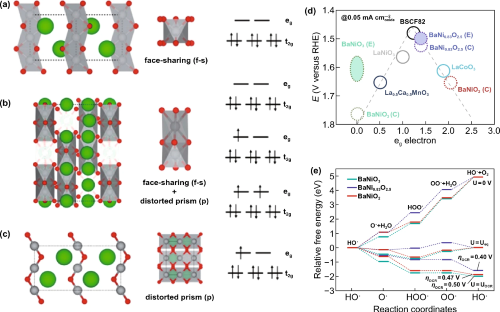
图7. BaNiO₃的相变示意图和OER活性的证据。(a) BaNiO₃晶体结构的示意图,其中显示了通过DFT计算得到的原子间距;(b) BaNi0.83O2.5晶体结构的示意图,其中显示了通过DFT计算得到的原子间距;(c) BaNiO₂晶体结构的示意图,其中显示了通过DFT计算得到的原子间距;(d) OER催化活性与过渡金属eg电子占据之间的关系,OER催化活性定义为0.05mA cm⁻²的OER电流过电位;(e) BaNiO₃、BaNi0.83O2.5和BaNiO₂的自由能图,取决于反应坐标。
V 缺陷工程
缺陷工程是一种已知的策略,用于设计更活性的氧电催化剂,包括OER、HER、ORR、氮还原反应(NRR)和CO₂还原(CRR)。在酸性介质中增加OER活性和稳定性的另一种方法是通过掺杂和掺杂剂淋洗来制备含缺陷的RuO₂。从有机框架生成的Cu掺杂RuO₂多面体多孔纳米晶体可能是通过产生氧空位来增加OER活性的最好示例(图8)。大部分在Cu附近产生的氧空位会导致相邻的Ru原子变得更为负电,从而将O 2p带的中心向费米能级移动,以实现更大的OER活性。Tian等人合成了掺杂Zn的RuO₂,并在酸性条件下进行了淋洗,制备了超细缺陷RuO₂(命名为UfD-RuO₂/CC)。所得到的催化剂在酸性环境中表现出优异的OER性能,在10 mA cm⁻²的电流密度下,过电位为179 mV,稳定性达20小时。强大的催化活性归因于活性位点和电子结构调控的协同影响。最近,人们还制备了一种掺杂钴的氧缺陷Ru基催化剂,其在10 mA cm⁻²的电流密度下,过电位为169 mV,持续50小时。OER性能的显著提高主要归因于氧空位和掺杂Co的RuO₂的改变电子结构,其使用了与空位相关的LOM途径,而不是AEM途径。为了探索氧空位在OER中的作用,研究了氧空位对相邻Ru原子的影响。通过比较LOM中的OvI和AEM中的5配位Ru之间的两种竞争性OER过程,探索了最优的自由能降低方法。
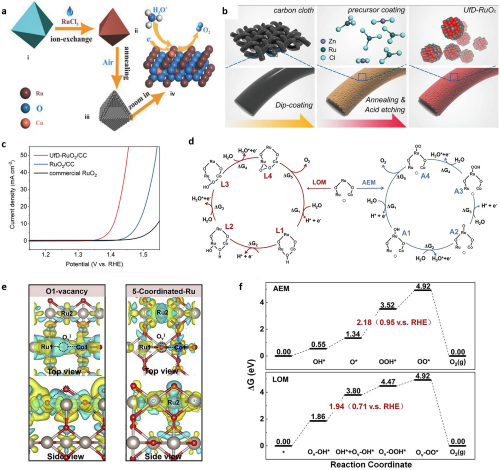
图8. (a) Cu掺杂RuO₂中空多孔聚形体的合成过程和模型的示意图。i)Cu-BTC多面体,ii)Ru交换的MOF衍生多面体,iii)超小Cu掺杂RuO₂纳米颗粒的中空多孔聚形体,iv)Cu掺杂RuO₂作为酸性环境中OER的电催化剂的扩展模型;(b) UfD-RuO₂/CC合成路线的示意图;(c) UfD-RuO₂/CC、RuO₂/CC和商业RuO₂/CC样品在氧饱和0.5M H₂SO₄溶液中具有相同质量负载后,经过电容校正和iR校正的OER极化曲线;(d) LOM和AEM机制的提出;(e) 通过A1和L1的电荷能差来说明OvI上电子消耗较Ru较少;(f) LOM和AEM的两种机制的自由能图。
在尖晶石中创造A位点的缺乏是增加氧电催化产生氧空位的一种方法,以促进氧电催化。邵教授的团队提出了一种简单有效的方法,将A位点阳离子缺乏引入到LaFeO₃钙钛矿中,以增加碱性溶液中的ORR和OER电催化活性,但是对于OER比ORR的增强更为显著(图9)。这种增加是由于表面氧空位和少量的Fe⁴⁺物种的形成,通过XPS证明了这一点,因为可以观察到La1-xFeO₃-δ的Fe 2p3/2峰轻微正移,表明铁处于较高的氧化态(+4)。穆斯堡尔谱学对铁敏感,常用于研究铁的电子结构。此外,原始的LF在穆斯堡尔谱中显示了单个Fe³⁺六重线分量,而A位点缺乏La1-xFeO₃-δ中出现了额外的Fe⁴⁺。氧空位缺陷的重要性迄今尚未被注意到,这使得晶体氧在钙钛矿表面是可移动的。钙钛矿晶体结构中氧的化学计量比例偏离了理论值3(化学式ABO₃),这会影响表面氧的可动性和材料的基础电子结构。空位生成的程度取决于氧的2p带和金属的3d带在晶体中的相互靠近程度,具有更多共价性的系统会显示出较大的空位浓度。随着钴离子的氧化态升高,其d轨道与O²⁻离子的s和p轨道有更高的重叠,从而产生π和σ带。Stevenson教授的团队引入了一些钴酸盐钙钛矿,通过将Sr²⁺掺入La1−xSrxCoO₃−δ中,以控制Co-O键的共价性和氧空位的数量。当Co的3d和O的2p带有足够的重叠时,就会产生氧空位,这表明空位参数中的基础电子结构。然后,氧空位会影响氧扩散速率,这与OER性能直接相关。
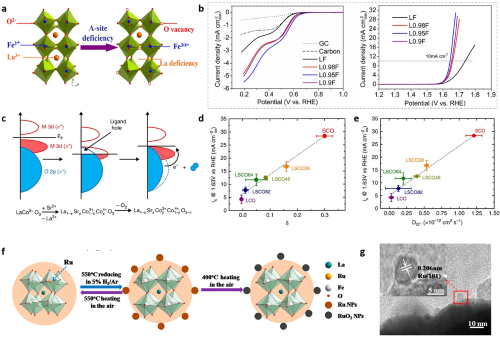
图9. (a) A位缺陷的La1-xFeO₃-δ钙钛矿中氧空位和Fe⁴⁺形成的示意图;(b) LF、L0.98F、L0.95F和L0.9F催化剂组成的RDE(1600 rpm)在氧饱和的0.1 M KOH溶液中进行ORR和OER的LSV曲线;(c) 氧空位浓度与La1-xSrxCoO₃中Co-O键共价性之间的关系;(d) 氧演化活性与缺陷参数δ的相关性;(e) 氧演化活性与氧离子扩散速率的相关性;(f) LFRO、Ru/LFRO和RuO₂/LFRO的晶格结构;(g) LFRO-550H的TEM图像,插图是Ru纳米粒子的析出。
VI 应力工程
应变工程是一种有效的方法,用于修改金属-氧键合能。晶格空位、畸变或不匹配所引起的晶格应变可以调控电子结构。拉伸应变和压缩应变是一种晶格应变,例如,在八面体配位下,分别促进了面内(dx²-y²)和面外(dz²)轨道的填充。Pesquera博士的团队揭示了ABO₃钙钛矿外延薄膜自由表面的对称性破缺效应,并表明它可以与衬底引起的外延应变相结合,随意调控面内和面外表面电子轨道的电子占据。在应变工程背景下,修改原子间距得到了广泛的研究。立方ABO₃钙钛矿的电子结构受到八面体结构(如B-O键长)的显著影响(图10)。应变对电子性质和化学性质都有影响。对于理想立方钙钛矿结构中的一行过渡金属钙钛矿氧化物,系统的DFT计算表明,对于早期过渡金属,增加d带宽度导致d带中心相对于费米能级的位置更高。这些计算假设在应变下d带电子填充恒定,并将d带近似为矩形形式。然而,对于晚期过渡金属,d带加宽会导致较高的d带填充,从而降低了d带中心。例如,对于放松的La₀.₆Sr₀.₄CoO₃结构的计算显示,在-3%到3%的双轴应变范围内,拉伸应变相对于费米能级引起了O 2p带中心的上移。因此,O 2p带中心在应变效应和各种物理和化学特性之间建立了关系。除了工作函数等电学因素外,O 2p带中心相对于费米能级的位置还与镧系钙钛矿中体相氧空位形成能量有关。由于应变对d带和O 2p带中心以及金属-氧重叠的影响,应变影响氧解离吸附能等表面性质。因此,应变调控可以影响电催化过程中的氧化物物种,从而改善氧电催化的速控步骤(例如在酸性OER中的HOO* →O*)。
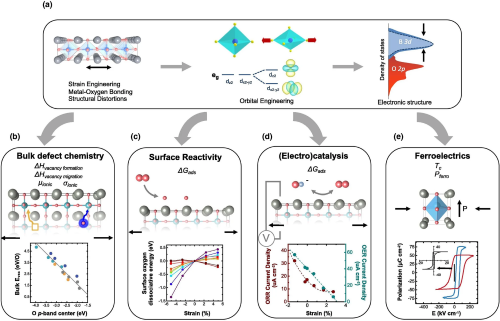
图10. 氧化物中应变、电子结构修改以及对氧化物功能的影响之间的相互作用。(a) 应变引起的结构修饰通过破坏对称性分裂了先前退化的能级,同时金属-氧轨道重叠的变化影响了电子态密度中d态的扩展;(b) 氧 2p能带中心上升与钙钛矿氧化物中体氧空位形成能降低之间的关联;(c) 钙钛矿氧化物的BO₂端处氧解离能的依赖性;(d) 在0.1 M KOH中,不同应变效应下LaNiO₃的室温ORR(0.823V RHE)与OER(1.623V RHE)的相关性;(e) 单晶BaTiO₃与生长在DyScO₃和GdScO₃上的BaTiO₃的极化行为对比。
从费米能级到氧态的电子传输的便利性随着氧的增加(去除)而增加(减少),以及它与体相中弱金属-氧键强度的关系,是造成氧空位形成能量降低的原因。应变通过改变O 2p带中心,相对于无应变的体相状态,来修改氧空位的形成能量。通过这种应变-缺陷连接,应变的结构效应与钙钛矿氧化物的化学离子性质相关联。来自应变对钙钛矿氧化物氧空位和间隙形成能量的影响可能会影响氧间隙抑制,特别是在Ruddlesden-Popper氧化物家族中。氧的迁移障碍通常由钙钛矿中的空位介导,这也受到应变的影响。在La2-xSrxNiO₄中,拉伸应变被发现可以降低氧和过氧化物间隙物种的间隙迁移障碍(图11)。拉伸应变的La1.85Sr0.15CuO₄(LSCO)的氧交换速率约比压缩应变膜提升了一个数量级。降低的氧间隙迁移障碍也可以应用于膜中的氧传输。在这些膜中,氧传输需要多个不同过程的协调,包括从分子态到晶格氧的氧交换的膜表面反应,以及同时的氧离子和电子传导(氧还原和演化)。例如,Pr2Ni1-xMoxO₄由于高间隙氧迁移性能而表现出优越的氧传输性能,氧扩散的障碍显著降低。此外,LaBO₃钙钛矿上氧和氧化物吸附物(*OH、*OOH)的吸附能也被观察到与O 2p带中心线性变化,使其成为OER和ORR过程中表面反应性的优秀电子结构描述符。
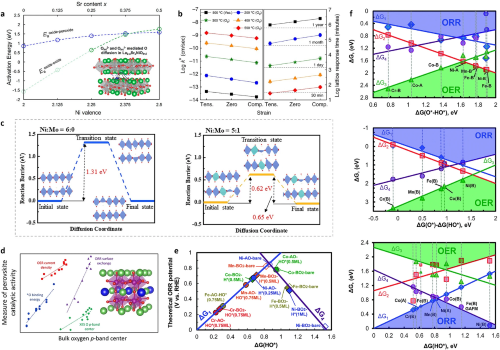
图11. (a) 氧化物-氧化物和氧化物-过氧化物扩散机制的激活能;(b) La1.85Sr0.15CuO₄的应变依赖性氧动力学。在不同退火条件和应变状态下,预测的氧表面交换速率k和吸收氧气所需时间的变化;(c) Pr2NiO₄和Pr2Ni5/6Mo1/6O₄晶格中氧的扩散路径(插图)和相应的扩散势垒;(d) 钙钛矿催化性能与氧p-带体描述符的相关性;(e) 理论ORR火山曲线;(f) 计算得到的ΔG1 (H₂O(l) + * → HO + H⁺ + e⁻), ΔG2 (HO* → O* + H⁺ + e⁻), ΔG3 (O* + H₂O(l) → HOO* + H⁺ + e⁻), 和 ΔG4 (HOO* → O₂(g) + H⁺ + e⁻)与ΔG(O*–HO*)之间的关系。
通过应变效应调控电子结构可以改变基元反应步骤中发生的质子-电子转移类型。在La0.8Sr0.2MnO₃-δ上形成Ba0.5Sr0.5Co0.8Fe0.2O₃-δ薄膜可以改善OER/ORR性能(图12)。Petrie等人通过外延拉伸导电钙钛矿LaNiO₃,研究其对ORR/OER的影响。这项工作表明,压缩应变显著改善了这两个过程,从而产生了优于贵金属的双功能催化剂。增强的双功能性归因于应变诱导的eg轨道分裂,填充面外dz2轨道,并改变钙钛矿BO₆八面体,修改表面轨道的不对称性。将应变应用于催化剂(例如钴酸盐和镍酸盐)以增加氧空位形成已被证明有益于构建更高活性的催化剂。当对SrCoO₃膜施加轻微的双轴拉伸应变2%时,氧空位形成的有利性(氧活化能障碍降低30%)表现为Co³⁺略微增加,CO⁴⁺减少。
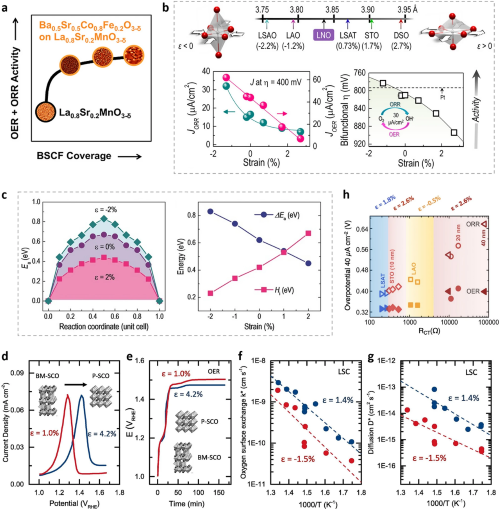
图12. (a) 用于氧电催化(ORR和OER)的双功能复合催化剂;(b) 通过压缩应变增强的ORR和OER双功能活性;(c) 应变依赖的氧活化;(d) 在10mV/s的扫描速率下,棕黑钙钛矿型SrCoO₂.₅ (BM-SCO) 被氧化成钙钛矿型SrCoO₃ (P-SCO) 时的阳极扫描;(e) 在不同拉伸应变下,5μA的恒流稳定性扫描在氧饱和的0.1 M KOH中进行;(f) La0.8Sr0.2CoO₃-δ (LSC)的温度依赖的k和 (g) D系数;(h) LCO上OER(实心圆)和ORR(空心圆)的过电位与不同拉伸应变(ε = 1.8%,2.6%,-0.5%)下的开路电流测得的电荷传递电阻(RCT)相关。
VII 氧电催化相关应用
探索高性能能源转换和储存(ECS)技术,如再生燃料电池、金属-空气电池和小分子(N₂、CO₂、H₂O)电解槽,能够在化学品中收集、转换和储存可再生能源,然后在需要的地方进行再转换,这是至关重要的,但仍然是一个科学挑战。因为它在将(可再生的)电能和化学燃料转化为电子的电化学反应中提供电子,所以OER和/或ORR模块是现代ECS系统中的关键组件。首先,在用于通过水分子电解生成化学燃料的电解槽的阳极发生OER(图13)。例如,水分解:氧电催化剂还可以用于水分解应用,其中水分解为氧气和氢气。这个过程用于生产燃料电池中使用的氢燃料。其次,氧电催化还用于金属-空气电池,其中氧气是阴极反应物。金属-空气电池具有高能量密度,正在作为传统锂离子电池的有希望的替代品进行开发。其中ORR发生在金属-空气电池的正极上,它的活性和稳定性影响着金属-空气电池的充放电性能。在各种氧化物催化剂中,钙钛矿催化剂作为双功能OER/ORR催化剂显示出出色的性能,有潜力用于锌空气电池。第三,氧电催化是燃料电池技术的关键方面。在燃料电池中,氧气在阴极处还原,产生水并产生电能。再生燃料电池可以在氢气生产(电解槽模式)和电能生产(燃料电池模式)两种模式下运行,只能通过氧电催化剂提供高效的长期能量储存和按需转换为电能。氧电催化剂在促进这一过程中发挥着关键作用,提高了燃料电池的效率和性能。与碱性OER相比,酸性OER更适用于商业化,因为质子交换膜(PEM)已成功开发并大规模应用,具有高质子传导率、高电压效率、低欧姆损耗、高电流密度和高气体纯度。更重要的是,酸性电解质相对于碱性电解质的固有优势在于,氢离子的电导率(350 S cm² mol⁻¹)远远高于氢氧根离子(198 S cm² mol⁻¹)。使用PEM技术的三种能量转换电解槽,例如水电解、氮还原和CO₂还原。与此同时,ORR主要与金属-空气电池和再生燃料电池有关。总的来说,氧电催化是一个关键的研究领域,在清洁能源生产、环境修复和化学合成等方面具有众多应用。

图13. 电化学能量转换和储能设备中的OER。(a) 用于小分子电解的电解器;(b) 金属-空气电池;(c) 再生燃料电池;(d) 依赖于质子交换膜的几种能量转换电解器示意图:水电解、氮还原和CO₂还原。
溶液中的氧电催化(OER和ORR)与固体氧化物燃料电池(SOFC)和固体氧化物电解池(SOEC)中的OER和ORR密切相关。除了水系中的氧电催化外,氧化物催化剂还广泛应用于SOFC和SOEC。OER和ORR与SOFC和SOEC之间存在密切的关系 (图14)。这四个过程都涉及氧分子的电化学反应。SOFC和SOEC是高效的能量转换和储存系统,能够实现高效的能量转换,包括OER和ORR是重要的反应。SOFC通过氢(或其他燃料)和氧反应产生电能、水和热,其中氧还原为氧离子。另一方面,SOEC通过电化学还原氧分子以产生氢或其他可燃气体,使用电能。因此,SOFC和SOEC本质上是OER和ORR的反向过程。在这些过程中,可以通过提高温度或施加电压来调整氧分子的活化能。通过提高温度或施加电压,氧分子的能量将增加,从而有助于降低OER和ORR反应的活化能,从而提高反应速率和效率。此外,作为催化剂的固体氧化物材料还可以通过调整其表面结构和电子性质来影响OER和ORR反应的速率和效率。
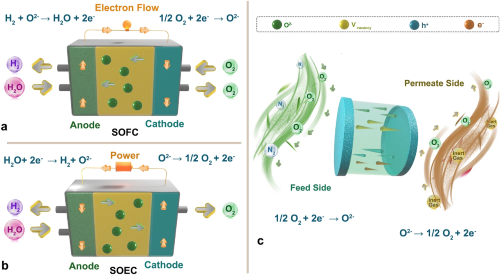
图14. (a) 固体氧化物燃料电池(SOFC)的工作原理示意图;(b) 固体氧化物电解池(SOEC)的工作原理示意图;(c) 基于混合离子-电子导体(MIEC)材料的氧分离膜的工作原理示意图。
VIII 总结与展望
总结而言,合理设计用于氧电催化的氧化物催化剂有潜力在各个领域引发革命性的变化,包括清洁能源生产和化学合成。通过了解氧化物催化活性背后的基本原理,研究人员可以设计出性能和耐久性更强的新型催化剂。设计氧化物催化剂的关键是调控它们的电子和几何结构。这可以通过元素掺杂、缺陷工程等技术实现。这些修改可以通过创建活性位点、增加表面积和优化催化剂的电子性质来增强氧化物的催化活性。此外,还可以探索具有独特性质的新型氧化物材料,如钙钛矿、尖晶石和层状双金属氢氧化物。这些材料具有高导电性、高比表面积和结构多样性等优点,可用于增强氧化物的催化活性。OER和ORR因其在各种能量转换和储存系统中的潜在应用而受到广泛关注,包括水电解器、金属-空气电池、电化学能量转换和储存系统。然而,尽管在氧化物催化剂的OER和ORR设计方面取得了重要进展,但仍然存在一些需要解决的挑战,以实现其广泛应用。
(a) 提高氧化物催化剂对ORR或OER的催化活性。虽然许多氧化物催化剂已被报道具有良好的ORR或OER活性,但其性能仍然不及贵金属催化剂。部分原因是ORR或OER的动力学缓慢和复杂的反应机理,需要高活性和选择性的催化剂。因此,有必要进一步研究ORR或OER过程的基本机制,以及如何通过调控来增强氧化物催化剂的活性。
(b) 提高氧化物催化剂在电化学设备恶劣工作条件下的稳定性。许多氧化物催化剂容易在电解质的腐蚀性、高温和高压条件下发生降解和失活。此外,氧化层和表面缺陷的形成也会导致催化活性随时间的推移而丧失。因此,需要开发新的合成和加工方法,以提高氧化物催化剂在这些条件下的稳定性和耐久性。
(c) 提高氧化物催化剂合成的可扩展性和成本效益。大多数氧化物催化剂是通过高温固相反应或溶胶凝胶法合成的,这些方法通常耗时、能耗高且难以扩大规模。因此,需要开发新的合成方法,可以低成本、大规模生产氧化物催化剂,同时保持其高活性和稳定性。
(d) 深入探究氧化物催化剂在氧电催化过程中的反应机制。应进行同位素示踪实验,研究真实的活性位点/中心和反应机制。例如,用于OER的氧化物催化剂将通过两种不同的反应机制发生:吸附物析出机制(AEM)和晶格氧介导机制或晶格氧氧化机制(LOM)。通过¹⁸O同位素检测反应产物以及密度泛函理论计算,可以研究合成催化剂的真实反应过程/机制。这将直接检测氧化物晶格中氧阴离子作为OER中的活性中介体的参与。
(e) 探索中间体有助于理解反应过程/步骤和真实机制。因此,建议进一步探索中间体,结合同位素示踪实验、理论计算和原位表征的直接证明。例如,原位衰减全反射表面增强红外吸收光谱(ATR-SEIRAS)测量对氧含中间体高度敏感,可用于OER和ORR研究。应进行更多原位表征实验,深入了解催化剂与催化性能(稳定性和活性)之间的真实关系,从晶相结构到氧化态。原位X射线吸收光谱(XAS)测量可用于原位氧化态探测,原位X射线吸收近边结构(XANES)对原位氧化态探测有用,原位扩展X射线吸收精细结构(EXAFS)对原位晶体探测有用。这些直接获取的信息有助于理解反应机制,从而指导有希望的催化剂的设计。
氧化物催化剂在电化学能量转换和储存系统中具有巨大的潜力,但在氧还原和氧发生反应的开发过程中存在重要挑战。提高氧化物催化剂的催化活性、稳定性和可扩展性对于它们的广泛应用和减少对化石燃料的依赖以及减轻能源生产对环境的影响至关重要。合理设计氧化物催化剂用于氧电催化是推动燃料电池、金属-空气电池、水电解和碳捕集技术发展的关键,这些技术可以显著减少温室气体排放,提高能源效率,并增强能源系统的可持续性。在这个领域持续进行研究对于实现更清洁和更可持续的未来至关重要。通过解决氧化物催化剂在ORR和OER方面的挑战,我们可以在迈向更清洁和更可持续的未来方面取得重要进展。这些催化剂的发展有可能彻底改变我们能源的生产和储存方式,从而使我们的能源系统更加高效和环保。因此,继续在这个领域投资研究对于发掘氧化物催化剂及其应用的全部潜力至关重要。
作者简介

本文通讯作者
▍主要研究成果
▍Email:xuanzhangzju@zju.edu.cn

本文通讯作者
▍主要研究成果
▍Email:lbxing@sdut.edu.cn

本文通讯作者
▍主要研究成果
▍Email:hao.tian@uts.edu.au

本文通讯作者
▍主要研究成果
▍Email:jan.fransaer@kuleuven.be
撰稿:原文作者
编辑:《纳微快报(英文)》编辑部
关于我们

如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 比利时鲁汶大学Jan Fransaer等综述:氧电催化中氧化物催化剂的设计—从机理到应用
 Nano-Micro Letters
Nano-Micro Letters