An integrated flexible bioelectrical and biochemical monitoring system based on spindle-structured directional sweat-pumping nanomesh
Jingzhi Wu, Rongkuan Han, Jianfeng Ma, Jinyi Gong, Tianxin Guan, Peiyan Dong, Hao Tang, Haidong Liu, Jinan Luo, Chang Liu, Yuanfang Li, Degong Zeng, Chuting Liu, Zhikang Deng, Xinyi Qu, Lvjie Chen, Tian-Ling Ren, Jianhua Zhou, and Yancong Qiao
Nano-Micro Letters (2026)18: 265
https://doi.org/10.1007/s40820-026-02115-w
本文亮点
1. 通过静电纺丝技术制备的纳米织物兼具润湿性和结构梯度特性,可实现高达4.00 mL min⁻¹ cm⁻²的超快单向液体传输速率。
2. 所构建的高透气透湿性纳米织物电极(ANE),具备皮肤保形性和可拉伸性,能在运动过程中稳定进行皮肤监测,同时具有优异的皮肤相容性。
3. 该系统实现无线连续电化学与电生理监测,融合汗液生物标志物与心电图(ECG)信号,实现全面健康分析。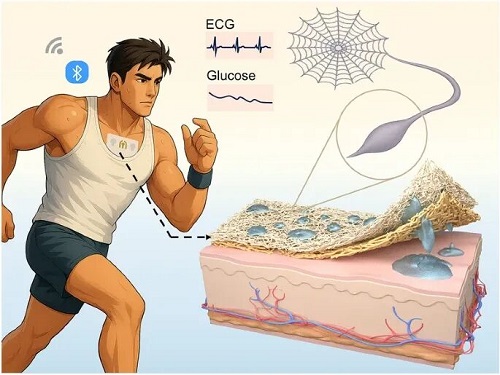
研究背景
柔性电子皮肤(e-skin)作为一种具备可拉伸性、柔软性和高贴合性的可穿戴设备,已逐渐成为可持续健康监测领域的一个重要发展方向。然而,现有的电子皮肤大多依赖于聚二甲基硅氧烷(PDMS)和聚对苯二甲酸乙二醇酯(PET)等致密基底材料,这些材料可能干扰皮肤与设备之间的热湿微环境,导致长期佩戴过程中舒适性下降,影响用户的佩戴体验和健康感知。此外,汗液积聚还可能削弱电极与皮肤的黏附性,进而影响信号采集的质量。为应对这些挑战,电子皮肤的研究正逐步向可渗透电子皮肤方向发展,特别是多孔结构纳米织物的研究。然而,现有工作大多通过材料本征孔隙率来提升透气性,尽管具备一定的渗透性,但其在排出汗液方面仍存在局限。为了解决这一问题,设计非对称性纳米织物成为一种有效的策略,这类设计能够实现定向液体传输,在需要长时间佩戴、对高透气性与排汗要求较高的场景中显示出巨大的应用潜力。
内容简介
现有电子皮肤面临着多种挑战,包括汗液积聚导致的贴合性不足、低透气性引起的佩戴不适以及信号获取类型的单一性,这些问题使得长期、稳定且高通量的信号记录成为一大难题。为了解决这些问题,中山大学周建华、乔彦聪及清华大学任天令团队采用静电纺丝技术构建了纺锤状结构的定向排汗纳米织物(SDSN)。通过调控纤维的形貌、孔径以及润湿性梯度等多维非对称性设计,SDSN能够高效定向传输汗液,其传输能力可达到典型人体排汗速率的1200倍。进一步地,该研究开发了基于定向排汗纳米织物的多模态生理监测系统,该系统实现了心电信号和汗液葡萄糖浓度的实时无线传输,为多模态个性化健康管理提供了有力支持。
图文导读
I 一体化多模态系统的设计
定向排汗多模态监测系统的总体设计如图1a所示,SDSN作为核心功能层,实现了汗液的单向传输。如图1b-c所示,SDSN的上下两层呈现出显著差异化的表面形貌:亲水性SF12层具有较小的孔隙,且形成了周期性纺锤结结构;而疏水性SF0层则由较粗且均一的纳米纤维构成,形成了较大的孔隙结构。在模拟出汗条件下,SDSN展现了高达4.00 mL×min⁻¹×cm⁻²的快速逆重力排汗传输速率,约为人体自然排汗速率的1200倍。系统进一步集成了封装在纳米织物中的检测电路与无线传输模块(图1f),在实现功能集成的同时保持了整体结构的水蒸气渗透性。该系统能够在身体活动过程中同步且稳定地记录ECG与汗液葡萄糖信号,具有优异的抗运动干扰性能,展示了其在实时多模态生理监测方面的先进能力。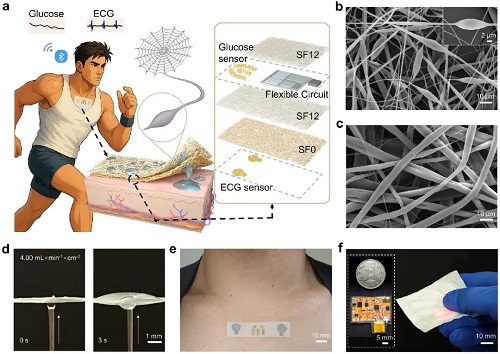
图1. 基于纺锤结构纳米织物的一体化多模态系统。a系统构成示意图。b SDSN中SF12层的SEM图像及纺锤结构的局部放大图。c SDSN中SF0层的SEM图像。d 在 4.00 mL×min⁻¹×cm⁻² 流量下,SDSN的逆重力输水过程。e 胸部佩戴的金纳米织物电极实物照片。f 纳米织物封装检测电路的实物照片。
II 纺锤结构定向排汗纳米织物的设计
SDSN采用了三重Janus设计,在润湿性、孔径和纺锤结构三个方面构建了不对称性。基于Rayleigh现象并结合低电压条件,研究团队成功制备出具有纺锤结构的纳米织物。尽管在传统静电纺丝过程中,珠状缺陷通常被视为不利因素,但该研究通过阐明纺锤结构在定向液体运输中的独特功能优势,将这一“缺陷”转化为具有实际应用价值的结构特征。在较低施加电压(13 kV)下,成功稳定地制备出纺锤结纳米织物;而当电压提高至19 kV时,获得了无纺锤结、直径更加均一的纳米织物。当从疏水侧滴加5 μL液体时,SDSN可在0.8秒内完成吸收及跨层传输,对应的单向传输速率约为6.25 μL×s⁻¹(图2c)。相比之下,缺乏纺锤结构的对照纳米织物完成同样体积的液体传输则需要13秒。同时,具有纺锤结构的织物展现出显著更高的横向铺展速率与垂直爬升速率(图2f-g)。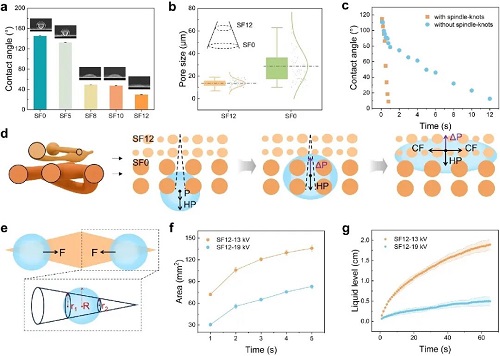
图2. SDSN的结构设计及其液体传输特性。a 不同SEBS/F127配比纳米织物的接触角(SFn表示SEBS:F127=(100−n):n)。b SF12层与SF0层的孔径对比。c 液滴自疏水层渗入纳米织物过程中接触角的变化。d SDSN逆重力液体传输机制示意图。e 由纺锤结构建的曲率梯度实现定向输水的原理。f 亲水纳米织物在有/无纺锤结构时的横向铺展面积曲线。g 亲水纳米织物在竖直浸润条件下,有/无纺锤结构时的液面爬升曲线。
III 双架构双视角的对比模型框架
由于液体渗透过程及其在纳米织物内部的动力学行为难以通过常规仪器直接观测,该研究建立了一个有限元仿真模型框架,用于模拟液体在纳米织物尺度上的驱动机制。研究构建了两类模型:一为均匀纳米织物模型(UNM),其顶部为无纺锤结的均一直径纳米织物层;二为纺锤状结构纳米织物模型(SNM)。模型从纵向和横向两个视角进行分析(纵向视角:SNM-l与UNM-l;横向视角:SNM-t与UNM-t)。仿真结果表明,SNM在两种视角下的逆重力液体传输速度均优于UNM:在纵向视角下,SNM的渗透速度提高了约1.3倍;在横向视角下,提升约4倍(图3e-f)。仿真与实验结果共同验证了纺锤结构能够在微纳尺度上建立多方向的表面能梯度,从而有效引导液体进行定向传输。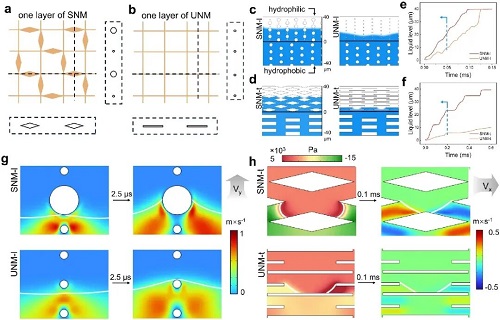
图3. 双架构双视角模型框架的分析。a、b SNM与UNM的俯视结构示意图,并分别给出从两种视角映射得到的单元结构示意。c SNM-l与UNM-l在0.05 ms时刻的液面位置,对应于图e。d SNM-t与UNM-t在0.2 ms时刻的液面位置,对应于图f。e 液体逆重力传输过程中,SNM-l与UNM-l的液面高度随时间变化对比。f SNM-t与UNM-t的液面高度随时间变化对比。g SNM-l与UNM-l在两个连续时刻的气液界面(白色线)处速度方向分量的分布。h SNM-t与UNM-t在气液界面处的压力分布及速度方向分量的分布。
IV 金织物电极的力学与生物相容性性能
该研究采用转移工艺从而将导电材料引入SDSN制备了ANE。ANE基于范德华力与汗液中的氢键作用实现电极与皮肤的贴合(图4a),能在扭转、弯曲与拉伸等多种形变条件下保持可靠的皮肤贴合性(图4b)。同时,ANE具备高可拉伸性,其伸长可接近自身长度的两倍(图4d),且在反复拉伸条件下具有优异的电学稳定性。其优越的透气透湿性能可以在运动过程中提供极佳的温度舒适性(图4g)同时不会引起皮肤刺激(图4h)。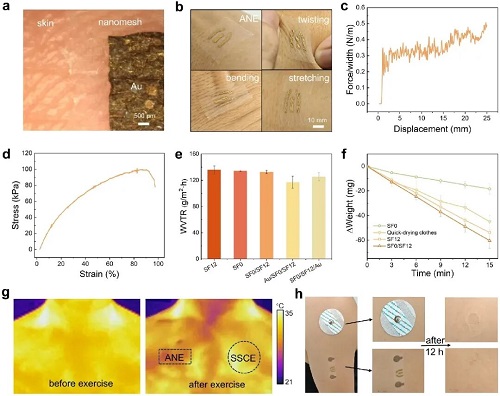
图4. ANE的性能表征。a ANE贴附于皮肤表面的实物照片。b ANE在扭转、弯曲与拉伸条件下的贴附状态。c 纳米织物的剥离力随位移变化的曲线。d 纳米织物的应力-应变曲线。e SF12(纯亲水纳米织物)、SF0(纯疏水纳米织物)、SF0/SF12(SDSN)、Au/SF0/SF12及SF0/SF12/Au的水分损失对比。f SF0/SF12(SDSN)、SF12、SF0与速干布料的液体蒸发速率对比。g ANE与Ag/AgCl电极(SSCE)的热舒适性测试结果。h ANE与SSCE的皮肤刺激性测试结果。
V 系统在心电与汗液葡萄糖监测中的应用
在电生理信号采集中,高渗透性、与皮肤的保形性以及低界面阻抗是确保信号完整性的关键因素。ANE的皮肤界面阻抗低于商用Ag/AgCl电极(0.63 MΩ vs 1.57 MΩ,1 Hz下),且在经历10次重复贴附剥离循环后仍能保持较低水平(图5a)。在出汗条件下,运动后ANE的信噪比相较于商用电极高出75%(图5c)。这些结果表明,ANE的定向排汗特性能够有效抑制汗液的积累并降低界面噪声,从而在热湿环境下提供更优的信号质量。除了电生理监测,ANE还可用于基于酶催化的汗液葡萄糖检测。该葡萄糖传感器展现出高灵敏度的电化学响应(图5e),并对汗液中常见组分具有较强的抗干扰性(图5f)。结合电生理和生化传感器技术与柔性电子技术,该研究构建了一种柔软、无线、且具有多模态功能的可穿戴监测系统。该系统整体厚度仅为4 mm,并且在包含电池与Ecoflex电路防水层的情况下总质量为2.61 g,体现了轻薄化与低负担佩戴特性。在运动过程中,系统测得的ECG信号质量保持一致,SNR始终维持在初始基线的90%以上(图5i)。此外,所测汗液葡萄糖水平成功反映了运动过程中能量摄入与消耗的动态变化(图5k),其变化趋势与商用动态血糖监测系统(CGM)测量结果一致。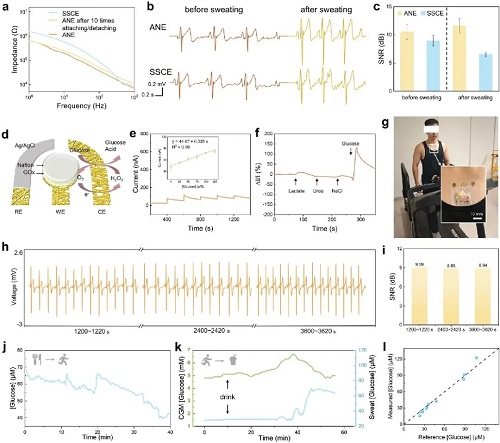
图5. 心电与汗液葡萄糖监测的应用。a SSCE、ANE及电极经10次贴附剥离循环后的皮肤-电极阻抗对比。b 两种电极在出汗前后采集的ECG记录对比。c 图b中ECG信号的SNR变化。d 基于ANE的电化学三电极结构示意图。e 传感器在0~125 μM葡萄糖浓度范围内的电流响应及浓度-电流拟合曲线。f 葡萄糖传感器的抗干扰实验。g 监测系统贴附于人体的实物照片。h 运动20、40与60 min时的连续ECG信号。i 运动20、40与60 min时ECG信号的SNR。j 餐后运动过程中汗液葡萄糖水平的变化。k 运动过程中能量补给引起的汗液葡萄糖变化,以及与CGM结果的对比。l 汗液葡萄糖测量值与参照值的对比。
VI 总结
该研究提出了一种基于纺锤结构排汗纳米织物的多模态监测系统,旨在解决电子皮肤在高温环境或高强度体力活动条件下所面临的透气性不足与排汗管理困难等关键挑战。通过在纳米织物中引入具有曲率梯度的纺锤结构,系统由单纯依赖材料化学性质的设计范式,转向微观结构与材料特性协同增强的策略。ANE的单向传输特性使其能够实现主动排汗泵送,并抑制来自外界的反向渗入,减少了电极滑移及其对ECG信号采集造成的干扰,与此同时,汗液可自发接触电化学电极以触发传感反应,并避免与皮肤直接接触,从而降低功能层受损风险。综上,该系统兼具舒适的佩戴体验与高质量的电生理及生化信号同步采集能力,可用于对生理状态与代谢活动进行更全面的评估,为构建更高集成度、更具用户自适应性与智能化的新一代可穿戴健康监测平台奠定了技术基础。
作者简介



关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2024 JCR IF=36.3,学科排名Q1区前2%,中国科学院期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 中山大学周建华/乔彦聪&清华大学任天令等:纺锤状定向导汗纳米网实现柔性生化电一体化监测系统
 Nano-Micro Letters
Nano-Micro Letters 福建师大陈桂林等:常压限域退火提升 Sb₂S₃薄膜太阳能电池结晶性与缺陷钝化
福建师大陈桂林等:常压限域退火提升 Sb₂S₃薄膜太阳能电池结晶性与缺陷钝化 NML卷期 | 2026年第5期免费下载
NML卷期 | 2026年第5期免费下载 清华大学邹贵生/刘磊等:325%可拉伸导体!仿生双尺度裂纹调控的金属薄膜导体用于 AI 电子皮肤
清华大学邹贵生/刘磊等:325%可拉伸导体!仿生双尺度裂纹调控的金属薄膜导体用于 AI 电子皮肤 NML封面文章|山东大学王桂龙等: 多功能Janus织物实现自适应热管理、自驱动感知与综合防护的一体化集成
NML封面文章|山东大学王桂龙等: 多功能Janus织物实现自适应热管理、自驱动感知与综合防护的一体化集成