Copper-Based Targeted Nanocatalytic Therapeutics for Non-Small Cell Lung Cancer
Yongfei Fan, Jiao Chang, Xichun Qin, Meng Li, Yan Li, Leilei Wu, Kun Li, Zhimin Chen, Yani Li, Zhongmin Tang*, Dong Xie*, Jianlin Shi
Nano-Micro Letters (2026)18: 152
https://doi.org/10.1007/s40820-025-01998-5
本文亮点
1. 开发了一种新型的Cu 纳米颗粒(NPs)——Cu与二巯丁二酸(DMSA)组装的NPs(Cu-DMSA NPs)。
2. NPs通过HA表面修饰(Cu-DMSA-HA NPs),选择性靶向癌细胞上过表达的CD44受体,并通过配位化学高效地催化生成ROS。
3. 这种高效的催化效应诱导了细胞内ROS的积累、线粒体损伤、GSH耗竭和谷胱甘肽过氧化物酶4(GPX4)下调,最终触发了癌细胞的铁死亡。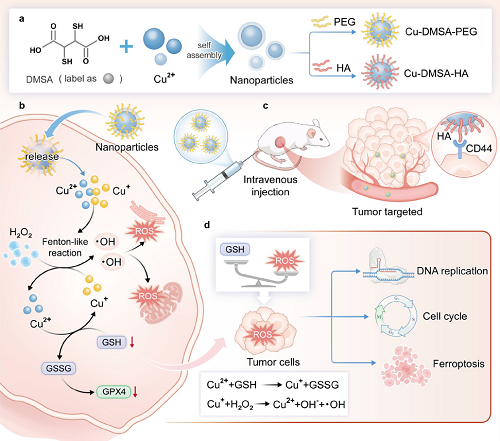
纳米颗粒(NPs)的制备及其抗肿瘤生物学机制示意图。
研究背景
肺癌是全球癌症相关死亡的首要原因,其中非小细胞肺癌(NSCLC)约占80%–85%。多数患者确诊时已处于中晚期,临床主要依赖化疗和免疫治疗。然而,化疗缓解率有限、耐药发生快且系统毒副作用显著,免疫治疗亦存在病理缓解率偏低等问题,严重制约了晚期NSCLC的整体疗效。因此,如何在降低全身毒性的同时实现肿瘤内高效杀伤,仍是亟待突破的临床难题。
近年来,受材料科学与纳米技术发展推动,基于氧化还原反应的纳米催化医学逐渐兴起,其通过在肿瘤微环境中原位催化产生活性氧(ROS),模拟并放大放疗和化疗的杀伤机制,从而实现更高治疗特异性。代表性的化学动力学治疗(CDT)利用内源性H₂O₂诱导类Fenton反应,但在实体瘤中常受限于肿瘤内高水平谷胱甘肽(GSH)的清除作用,以及传统Fe基催化剂在弱酸性或近中性条件下催化效率不足等问题。
长期以来,如何同步突破肿瘤抗氧化防御并维持高效、持续的ROS催化,是纳米催化医学面临的关键科学瓶颈。相较之下,铜基纳米催化体系可被GSH还原并驱动高效类Fenton反应,在消耗抗氧化物质的同时实现持续ROS放大,为克服NSCLC内在耐受性提供了新的研究方向。
内容简介
常规治疗NSCLC面临缓解率低、耐药性强和严重副作用等问题。为了充分利用ROS的治疗潜力,纳米催化医学利用纳米材料在肿瘤部位特异性生成ROS,从而实现高效、靶向的癌症治疗。在本研究中,同济大学施剑林院士、谢冬、唐忠敏等人开发了Cu-DMSA-HA NPs,制备的纳米颗粒不仅具有肿瘤靶向能力,同时具备通过配位化学高效催化ROS生成。HA表面修饰通过识别癌细胞上过表达的CD44受体,促进靶向递送,增强纳米颗粒的摄取。一旦进入细胞,纳米颗粒会消耗细胞内的GSH,随后通过类Fenton反应维持ROS的生成。体内外实验表明,这种催化策略有效抑制肿瘤细胞DNA复制,阻滞细胞周期进程,下调GPX4表达,诱导铁死亡,最终抑制NSCLC的进展。总体而言,该研究为纳米催化医学在肺癌治疗中的应用提供了新思路,也展示了“靶向+催化+铁死亡”协同策略的巨大潜力。
图文导读
I 新型铜基纳米颗粒:可靶向、可响应、可催化的“智能”抗癌平台
该研究团队设计并合成了一种新型铜配位纳米颗粒(Cu-DMSA-HA NPs),其核心由铜离子与DMSA通过配位作用构建。通过调整铜与DMSA的比例,发现1:1配比时能够得到分散良好、粒径约18 nm的纳米颗粒;而铜离子过多或DMSA过量会导致颗粒聚集或分解,稳定性显著下降。为提升体内循环稳定性与肿瘤靶向性,他们进一步在颗粒表面修饰HA,其中Cu-DMSA-HA NPs水合粒径约24 nm,呈椭圆形,表面带负电荷,元素分布均匀,表征结果表明材料合成成功。
更为重要的是,该团队发现Cu-DMSA-HA NPs具有显著的类Fenton催化活性:在 H₂O₂存在时能够快速产生大量羟基自由基(·OH),实现高效ROS生成;在还原性分子GSH作用下,纳米颗粒发生解体并进一步增强催化活性,呈现出“GSH响应型”的结构降解与活性提升特征。此外,该纳米材料在酸性环境(pH 5.5)中催化能力更强,符合肿瘤微环境的酸性特征。该平台不仅稳定可储存,还具备靶向、响应与高效催化三重优势,为肿瘤治疗提供了新的可控策略。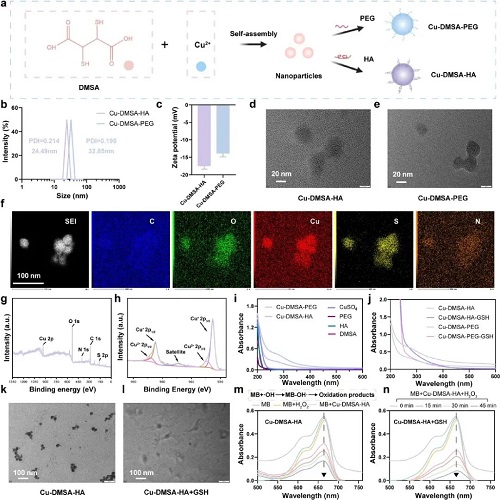
图1. Cu-DMSA-HA NPs的制备与表征。
II Cu-DMSA-HA NPs“精准”靶向NSCLC细胞并诱导肿瘤细胞凋亡
研究团队基于HA可高亲和结合肿瘤细胞表面CD44受体的特性,进一步验证了Cu-DMSA-HA NPs对NSCLC的选择性杀伤作用。细胞实验显示,Cu-DMSA-HA NPs在不同NSCLC细胞系(PC-9、NCI-H460、NCI-H322、A549、NCI-H1975)中呈剂量依赖性抑制细胞增殖,并在40 μg/mL时对PC-9和NCI-H1975细胞表现出最强敏感性;而正常支气管上皮细胞BEAS-2B在相同条件下仍保持高存活率,显示出明显的肿瘤选择性毒性。与Cu-DMSA-PEG NPs相比,Cu-DMSA-HA NPs在相同浓度下对癌细胞的抑制效果更显著,而对正常细胞的毒性更低,证明其具有更优的生物安全性和靶向优势。
进一步的共聚焦显微成像显示,Cu-DMSA-HA NPs在肿瘤细胞周围的累积明显高于Cu-DMSA-PEG NPs,提示HA介导的CD44识别提升了靶向能力。通过siRNA敲低CD44后,Cu-DMSA-HA NPs的细胞摄取显著下降,证实其靶向机制依赖CD44。活死染色与流式细胞术结果均表明,Cu-DMSA-HA NPs可显著增加肿瘤细胞的早晚期凋亡比例,抗肿瘤效果优于Cu-DMSA-PEG NPs。值得注意的是,尽管Cu-DMSA-HA NPs中铜含量更低,但其抗肿瘤效果更强,进一步证明其通过增强肿瘤细胞摄取而实现了更高的治疗效率。该研究为NSCLC提供了一种更安全、更高效的靶向治疗策略。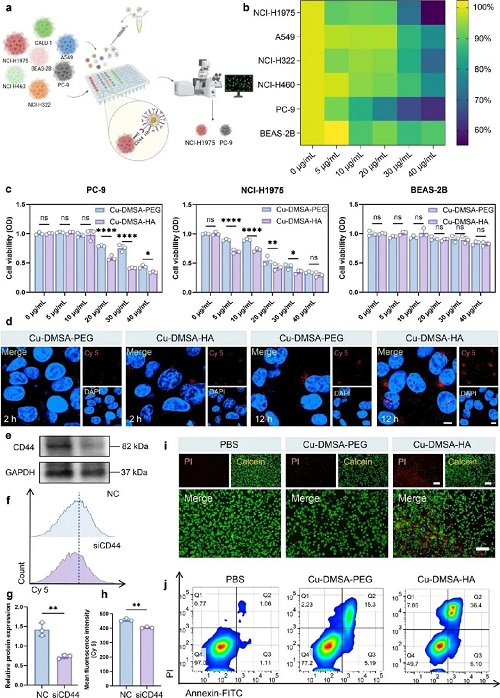
图2. Cu-DMSA-HA NPs体外靶向肿瘤细胞并且诱导细胞凋亡能力。
III 转录组测序(RNA-seq)联合单细胞RNA测序(scRNA-seq)揭示Cu-DMSA-HA NPs诱导NSCLC细胞凋亡的机制:恢复铁死亡,打破肿瘤“抗压”屏障
该研究团队进一步通过RNA-seq与scRNA-seq解析Cu-DMSA-HA NPs对NSCLC细胞的作用机制。RNA-seq结果显示,Cu-DMSA-HA处理组与对照组相比,下调基因主要涉及细胞周期和DNA复制等与肿瘤增殖相关的通路,而上调基因则富集于蛋白折叠、未折叠蛋白反应及内质网应激等过程,这些均是氧化应激的典型特征。通路分析进一步显示,蛋白加工和铁死亡相关通路被显著激活。
值得注意的是,研究发现促铁死亡关键基因ACSL4和SLC7A11显著上调,而抑制铁死亡的关键基因GPX4显著下调,提示Cu-DMSA-HA可能通过氧化应激破坏红氧稳态,诱导肿瘤细胞发生铁死亡。为探究其在肿瘤与正常细胞中的差异调控,团队整合了NSCLC单细胞数据,对上皮细胞亚群重聚类后发现,恶性上皮细胞具有明显的基因组拷贝数变异(CNV)并表现出更强的增殖信号,同时其铁死亡相关信号普遍被抑制,GPX4活性更高,显示肿瘤细胞天然具有“抗铁死亡”能力。
总体而言,RNA-seq与scRNA-seq联合分析揭示,Cu-DMSA-HA NPs可通过诱导氧化应激,恢复NSCLC细胞的铁死亡通路,从机制层面解释了其肿瘤选择性杀伤作用,为NSCLC靶向治疗提供了新的思路。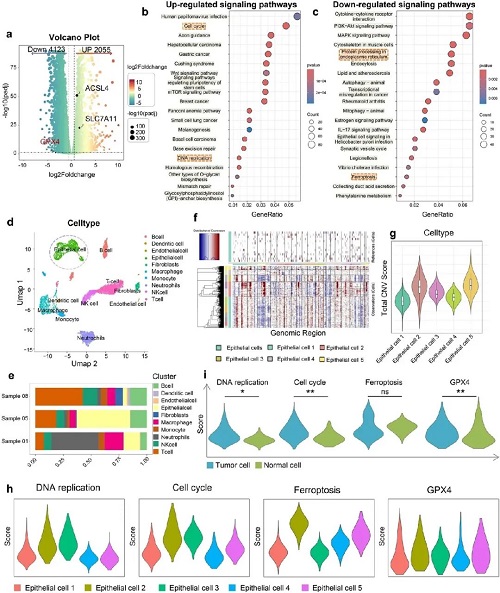
图3. RNA-seq联合scRNA-seq分析揭示Cu-DMSA-HA NPs的抗肿瘤机制。
IV 多项体外实验表明Cu-DMSA-HA NPs具有优秀抗NSCLC增殖与转移的能力
研究团队进一步在细胞水平验证了Cu-DMSA-HA NPs的抗肿瘤作用。EdU实验显示,Cu-DMSA-HA NPs显著抑制PC-9和NCI-H1975细胞的DNA复制能力,其抑制效果明显优于Cu-DMSA-PEG NPs。克隆形成实验也证明,Cu-DMSA-HA NPs显著降低了NSCLC细胞的克隆形成能力,进一步证实其抑制增殖的强效作用。
在迁移与侵袭方面,伤口愈合实验显示Cu-DMSA-HA NPs显著抑制肿瘤细胞迁移能力,效果优于Cu-DMSA-PEG NPs。Transwell实验也一致表明其能够显著降低NSCLC细胞的侵袭与迁移能力,提示其具有抑制肿瘤转移潜能。
此外,细胞周期分析显示,Cu-DMSA-HA NPs可诱导PC-9和NCI-H1975细胞在G2/M期停滞,且停滞程度高于Cu-DMSA-PEG NPs,说明其可通过阻断细胞周期进程来抑制肿瘤增殖。
综合而言,Cu-DMSA-HA NPs不仅能有效抑制NSCLC细胞增殖,还可显著阻断其侵袭、迁移及细胞周期进程,展现出作为NSCLC潜在治疗药物的强大前景。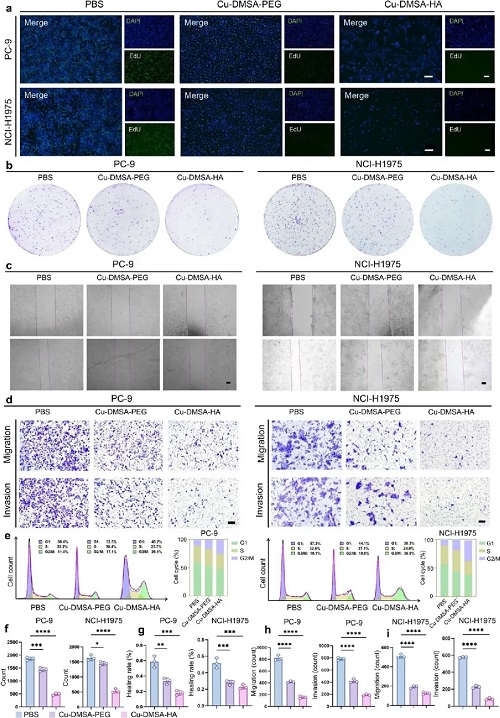
图4. Cu-DMSA-HA NPs抑制NSCLC细胞恶性生物学行为。
V Cu-DMSA-HANPs通过氧化应激“点燃”铁死亡抑制NSCLC进展
研究团队进一步揭示,Cu-DMSA-HA NPs能够在肿瘤细胞内通过类Fenton反应持续产生ROS,触发强烈氧化应激。RNA测序显示,Cu-DMSA-HA NPs处理后,NSCLC细胞中氧化应激与铁死亡相关通路显著上调。细胞实验也表明,Cu-DMSA-HA NPs在PC-9和H1975细胞中诱导更高水平的ROS积累,并导致线粒体膜电位下降、结构损伤及细胞形态异常,提示启动线粒体依赖性细胞死亡。与此同时,Cu-DMSA-HA NPs显著降低细胞内GSH/GSSG比值并下调抗氧化酶GPX4,导致脂质过氧化加剧,C11-BODIPY染色显示脂质ROS大量积累。重要的是,铁死亡抑制剂Fer-1可显著逆转脂质ROS积累并恢复细胞活力,证实Cu-DMSA-HA NPs的细胞死亡主要由铁死亡驱动。
此外,团队还分析了不同NSCLC细胞系对Cu-DMSA-HA NPs的敏感性差异,发现PC-9和H1975细胞具有更高的CD44和ACSL4表达,同时内源性抗氧化能力(GSH/GSSG比值)较弱,解释了其更易被Cu-DMSA-HA NPs“击中”。这些分子特征可作为潜在生物标志物,帮助筛选更可能受益的患者人群。整体而言,Cu-DMSA-HA通过破坏红氧平衡、诱导铁死亡,为NSCLC提供了一条可控且高效的治疗新策略。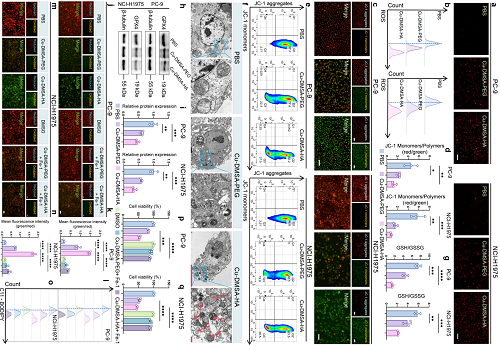
图5. Cu-DMSA-HA NPs在NSCLC中诱导氧化应激并且激活铁死亡。
VI Cu-DMSA-HA NPs在体内“精准”靶向NSCLC肿瘤组织:肿瘤部位持续富集并且非靶器官快速清除
研究团队在体内验证了Cu-DMSA-HA NPs的靶向能力与安全性。血液相容性实验显示,该纳米颗粒在高达2.5 mg/mL浓度下无溶血风险,适合静脉注射。小鼠肿瘤模型的实时荧光成像表明,Cu-DMSA-HA NPs在注射后8小时内持续在肿瘤部位累积,并在24小时内显著高于Cu-DMSA-PEG NPs与游离染料,且肿瘤富集可维持至72小时,显示出优异的肿瘤靶向与滞留能力。药代动力学结果进一步证实,Cu-DMSA-HA NPs具有更长的体内停留时间和更高的系统暴露。脏器分布与免疫荧光分析显示,纳米颗粒在肺和肾脏短暂积累后逐渐清除,而心、肝、脾等关键器官信号极低,提示非靶向毒性较小。总体而言,Cu-DMSA-HA NPs具备高效肿瘤靶向、长效滞留与快速代谢清除的优势,为NSCLC体内治疗提供了可靠基础。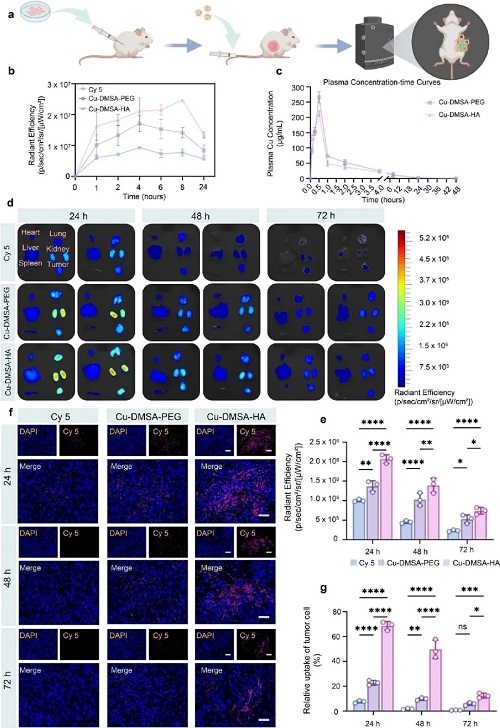
图6. Cu-DMSA-HA NPs体内肿瘤靶向和器官清除能力评估。
VII Cu-DMSA-HA NPs在体内通过氧化应激诱导肿瘤细胞铁死亡抑制NSCLC进展和肺部转移
在确认了Cu-DMSA-HA NPs良好的体内分布与肿瘤靶向性后,研究团队进一步在PC-9肿瘤小鼠模型中评估其治疗效果。结果显示,与PBS对照组相比,Cu-DMSA-HA NPs显著抑制肿瘤生长,并且抗肿瘤效果优于Cu-DMSA-PEG NPs。肿瘤切除后的组织分析也一致支持这一结论。组织学染色结果显示,Cu-DMSA-HA可明显降低肿瘤细胞增殖标志物Ki-67的表达,并通过下调GPX4、增强ROS积累等方式诱导铁死亡,TUNEL染色进一步证明其显著增加肿瘤细胞凋亡,且效应强于Cu-DMSA-PEG NPs。
为了评估对晚期转移性NSCLC的疗效,团队建立了肺转移模型。结果表明,Cu-DMSA-HA NPs显著减少肺部转移灶体积,且优于Cu-DMSA-PEG NPs与PBS组,显示出抑制转移的潜力。
此外,研究团队还比较了Cu-DMSA-PEG NPs与一线化疗药顺铂在NSCLC中的疗效与安全性。结果显示,Cu-DMSA-PEG NPs显著抑制肿瘤生长且肿瘤负荷低于顺铂。更重要的是,顺铂组出现体重下降、血液毒性和肝肾损伤,而Cu-DMSA-PEG NPs组无明显毒性,展示出更高效且更安全的治疗潜力。
总体而言,Cu-DMSA-HA在体内不仅能有效抑制肿瘤生长,还可通过诱导氧化应激与铁死亡,显著降低转移风险,展现出作为NSCLC治疗新策略的强大潜力。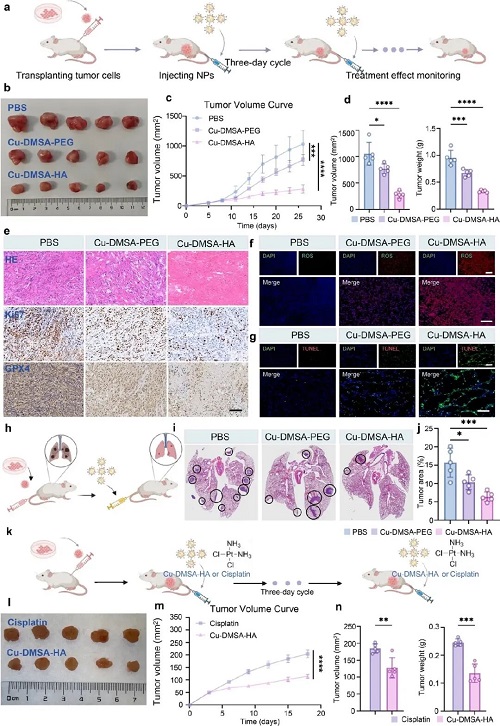
图7. Cu-DMSA-HA NPs体内抗肿瘤疗效评价。
VIII 总结
在这项研究中,团队提出了一种简便可控的制备策略,构建了具有肿瘤靶向性的铜基纳米颗粒Cu-DMSA-HA NPs,用于通过GSH耗竭与类Fenton反应诱导ROS生成,治疗NSCLC。该纳米颗粒由DMSA配位组装而成,并通过HA修饰实现对肿瘤细胞表面高表达CD44受体的主动识别与摄取。进入肿瘤细胞后,Cu-DMSA-HA NPs与胞内GSH反应生成大量Cu(I),进一步触发类Fenton反应,持续产生ROS并导致氧化应激增强。转录组RNA-seq分析显示,Cu-DMSA-HA NPs显著抑制癌细胞DNA复制与细胞周期进程,同时激活铁死亡通路;体内外实验亦证实其可显著降低GSH/GSSG比值、抑制GPX4活性,最终诱导NSCLC细胞发生铁死亡。
与已有铜基纳米平台相比,Cu-DMSA-HA NPs具备三大优势:一是制备简单、可重复;二是HA实现CD44介导的主动靶向,区别于多数非靶向材料;三是“GSH耗竭→类Fenton反应”顺序催化机制,确保持续ROS释放与高效铁死亡诱导,显著提升治疗效果。研究结果表明,该纳米体系在皮下与原位肺癌模型中均能选择性抑制肿瘤进展,并具备良好生物相容性。尽管仍需进一步评估长期安全性与耐药风险,但作为纳米催化医学的代表,Cu-DMSA-HA NPs展现出明确的临床转化潜力,有望为患者带来新的治疗选择。
作者简介



关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2024 JCR IF=36.3,学科排名Q1区前2%,中国科学院期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 同济大学施剑林院士、谢冬、唐忠敏等:新型铜基纳米催化剂精准“点燃”非小细胞肺癌铁死亡
 Nano-Micro Letters
Nano-Micro Letters 中科院赣江创新研究院彭立山/余建敏等:提升OH⁻选择性吸附实现大电流持久海水电解
中科院赣江创新研究院彭立山/余建敏等:提升OH⁻选择性吸附实现大电流持久海水电解 东华大学缪月娥/张辉&上海交大赖飞立等: 面向固态锂电池的“离子门控”聚多酚复合电解质,重塑有机-无机界面
东华大学缪月娥/张辉&上海交大赖飞立等: 面向固态锂电池的“离子门控”聚多酚复合电解质,重塑有机-无机界面 香港城大Duu-Jong Lee团队:面向可持续规模化有机光伏的 Y 系受体自组装调控
香港城大Duu-Jong Lee团队:面向可持续规模化有机光伏的 Y 系受体自组装调控 香港理工徐正龙等:铁锰双掺杂精准调控NVPF电子结构提升钠离子电池性能
香港理工徐正龙等:铁锰双掺杂精准调控NVPF电子结构提升钠离子电池性能