Phage-Inspired Artificial Peroxidases with Robust Sub-nanometer Cluster Sites for Efficient Oral Biofilm Elimination and Dental Caries Prevention
Huang Zhu, Ting Wang, Shihuan Gao, Wei Geng, Tian Ma, Liang Cheng, Xianglong Han, Jiuhong Deng*, Shanshan Gao*, and Chong Cheng*
Nano-Micro Letters (2026)18: 303
https://doi.org/10.1007/s40820-026-02138-3
本文亮点
1. 仿生拓扑,酶活强劲: 受噬菌体抗菌机制启发,从头设计出具有尖刺拓扑结构的仿生人造酶材料。其表面稳固的Ir亚纳米簇位点赋予了材料极强的酶活性,能够高效捕获并清除浮游状态的变异链球菌,从源头上抑制口腔生物膜形成。
2. 防蛀抗蚀,效果明显: 利用Ir簇酶强大的催化活性与尖刺表面的物理拓扑优势协同作用,在防龋实验中显著抑制牙齿表面生物膜的生成,有效防止牙釉质脱矿,并大幅降低龋齿发生率,展现出极具潜力的临床防龋应用价值。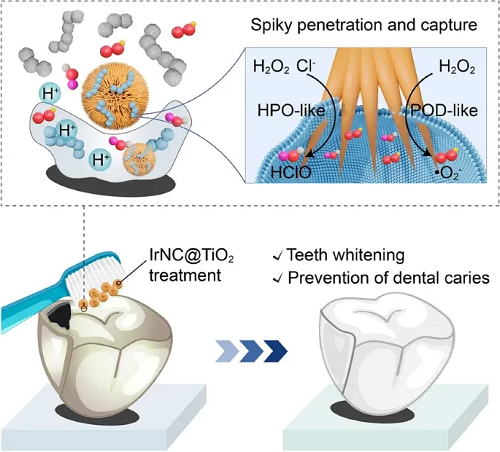
研究背景
龋齿(Dental caries)研究现在大家都在关注:各种不同的抗菌材料、酶模拟策略、生物膜破坏技术、纳米酶设计、防龋涂层,等等。尤其对于口腔生物膜,必须同时考虑清除浮游细菌和瓦解已形成的致密基质,而不是只侧重其中一方。变异链球菌(S. mutans)代谢产酸形成的胞外聚合物(EPS)基质具有物理屏障功能,既阻碍抗菌药物渗透,又限制活性氧(ROS)的扩散与作用时效(ROS半衰期<200 ns,扩散范围~20 nm)。此外,常规研究往往聚焦于对浮游细菌的杀灭效果,却忽视了在生物膜完全形成后,EPS屏障会变得愈发致密顽固,如何对其进行有效破坏,是通往临床防龋应用道路上一个更具挑战性的课题。长期以来,如何实现同步解决生物膜屏障的物理阻隔与ROS的有限作用距离这两大顽疾,是该领域的关键科学瓶颈。
内容简介
针对口腔生物膜清除中浮游细菌杀灭与致密EPS基质破坏难以兼顾、传统仿生仿酶ROS催化材料作用距离有限且难以穿透生物膜屏障的关键瓶颈,四川大学程冲教授团队跳出以往“单点设计”(仅优化酶活性或仅优化材料形貌)的框架,通过模仿噬菌体的结构与抗菌特征,实现了人造酶材料对催化活性与物理破膜能力的协同集成并设计了一种新型仿噬菌体人造酶材料(IrNC@TiO₂),其核心创新在于一举两得:一方面,海胆状尖刺拓扑结构赋予材料机械破膜能力,可有效捕获并物理破坏致密的生物膜EPS基质;另一方面,稳定锚定于TiO₂表面的亚纳米Ir簇通过Ir–O配位作用实现了高效、稳定、多酶模拟的ROS催化活性,持续产生超氧自由基(•O₂⁻)和次氯酸(HClO),实现对浮游变异链球菌的高效清除。该策略无需复杂的材料修饰或多种组分复合,仅通过单一杂化体系中的形貌-活性协同设计,同步攻克了生物膜物理屏障阻隔与ROS作用范围受限这两大核心瓶颈,并在动物龋齿模型中验证了其抑制牙釉质脱矿、降低龋齿发生率的临床潜力,为口腔健康防护用高效ROS催化平台的设计提供了新思路。
图文导读
I 仿生双引擎:物理捕菌与化学杀灭的协同作战
如图1所示,该仿噬菌体人造酶材料(IrNC@TiO₂)在口腔生物膜清除中上演了一场“物理-化学”双引擎协同作战。在物理层面(图1a),其海胆状尖刺拓扑结构模仿了噬菌体捕获细菌的尾丝机制,通过纳米尺度的尖刺有效捕获、锚定并物理破坏致密的生物膜胞外聚合物(EPS)基质,打破了传统ROS难以穿透的屏障。在化学层面(图1b),稳定锚定于TiO₂表面的亚纳米Ir簇通过Ir–O配位作用,持续催化产生超氧自由基(•O₂⁻)和次氯酸(HClO),实现对被捕获变异链球菌的高效杀灭。二者协同作用,使得该材料在作为牙膏添加剂时(图1b),不仅能有效清除牙齿表面的生物膜、实现牙齿美白,更能从根本上降低龋齿发生风险。
图1. 本文提出的仿噬菌体人造酶材料用于生物膜抑制和龋齿预防示意图。
II 结构设计:从尖刺基底到亚纳米Ir簇的精准构筑
本研究成功合成了仿噬菌体人造酶材料(IrNC@TiO₂)。 以溶剂热法合成的尖刺状TiO₂(S-TiO₂)为基底,通过水热离子交换及300 °C氩气退火,获得了亚纳米Ir簇均匀锚定的人造酶材料。结构表征表明IrNC@TiO₂中Ir以亚纳米簇(平均0.92 nm)形式高分散于TiO₂表面。HAADF-STEM、EDS mapping及XPS证实Ir通过Ir–O配位稳定锚定于TiO₂,形成电子界面。XANES分析显示Ir平均价态为+1.32,EXAFS及小波变换进一步确认了Ir–O及Ir–Ir配位共存。此外,IrNC@TiO₂较TiO₂具有显著降低的Zeta电位,赋予其更优的分散稳定性。综上,亚纳米Ir簇通过Ir–O–Ti配位框架稳定锚定于海胆状TiO₂表面,为后续高效抗菌及防龋应用提供了结构基础。
图2. IrNC@TiO₂的制备及形貌结构表征。
III 酶学引擎:亚纳米Ir簇驱动的高效活性氧产生
本研究系统表征了IrNC@TiO₂的类过氧化物酶(POD)及类卤过氧化物酶(HPO)活性。以TMB为分子探针,IrNC@TiO₂在H₂O₂存在下表现出优异的类POD活性,且活性随pH变化。循环测试表明,该材料经过6次反应后仍保持高活性,稳定性优异。稳态动力学分析显示,与IrNP@TiO₂相比,IrNC@TiO₂具有更高的最大反应速率(87.26 × 10⁻⁸ M s⁻1)和周转数(308.30 × 10⁻3 s⁻1),以及更低的米氏常数(2.12 mM),表明亚纳米Ir簇对H₂O₂具有更高效的催化动力学和亲和力。与近期报道的类POD仿酶材料相比,IrNC@TiO₂的TON值位居前列。活性氧(ROS)种类鉴定表明,IrNC@TiO₂催化产生的主要ROS为超氧自由基(•O₂-)。 采用HE探针及电子顺磁共振(EPR)证实,IrNC@TiO₂产生的•O₂-量显著高于IrNP@TiO₂,且未检测到显著的•OH或1O₂生成。进一步发现IrNC@TiO₂具有卤过氧化物酶(HPO)样活性,可在H₂O₂和Cl⁻存在下催化生成次氯酸(HClO)。通过CB探针及APF探针检测,IrNC@TiO₂的HPO催化活性显著优于IrNP@TiO₂及纯S-TiO₂。
密度泛函理论(DFT)计算揭示了IrNC@TiO₂催化生成•O₂-和HClO的最优反应路径。 对于POD仿酶催化过程,最合理的路径涉及OH*在Ir和相邻Ti原子上的共吸附,决速步能垒仅为0.51 eV。对于HPO仿酶催化过程,最合理的路径决速步能垒低至0.17 eV。理论计算与实验观测高度吻合,证实了亚纳米Ir簇与TiO₂基底之间的协同催化机制。
图3. IrNC@TiO₂的仿酶催化性能评价及路径分析。
IV 细菌捕获与杀灭:尖刺介导的物理穿孔与ROS化学损伤
本研究通过分子动力学(MD)模拟、抗菌实验及形貌观察,系统揭示了IrNC@TiO₂海胆状尖刺结构对变异链球菌(S. mutans)的捕获与杀灭机制。MD模拟表明, 与平面TiO₂无法穿透脂质双层不同,尖刺TiO₂结构能够自发刺入并持续破坏细菌膜。相互作用能分析证实,尖刺结构进入细胞膜为自发过程,而平面结构则难以实现膜穿透,从理论上解释了尖刺形貌增强细菌捕获能力的物理基础。抗菌活性评估显示, IrNC@TiO₂在200 μg·mL⁻1浓度下可完全抑制浮游S. mutans生长。通过对比实验发现:无酶活性的球形TiO₂(C-TiO₂)抑菌率仅约14%;单纯依靠尖刺物理作用的S-TiO₂抑菌率达约75%;而兼具尖刺形貌与酶催化活性的IrNC@TiO₂联合H₂O₂处理后,抑菌率接近99%,充分证明了物理捕获与ROS化学杀灭的协同增效作用。Live/Dead染色、SEM及TEM观察进一步证实, IrNC@TiO₂的纳米尖刺能够诱导细菌包膜变形与穿孔,导致膜电位丧失及胞质内容物泄漏。蛋白泄漏实验显示IrNC@TiO₂组蛋白泄漏量最高,证实了严重的膜完整性破坏。综上,IrNC@TiO₂通过尖刺结构的物理捕获与膜穿孔、以及酶催化产生的ROS化学损伤双重机制,实现了对浮游S. mutans的高效清除。
图4. IrNC@TiO₂抗游离变形链球菌性能评价。
V 破膜双刃:尖刺穿透与ROS瓦解生物膜屏障
本研究系统评估了IrNC@TiO₂对变异链球菌生物膜的清除能力,并通过分子动力学模拟揭示了其穿透机制。CLSM成像显示, IrNC@TiO₂处理组中约72%的生物膜相关细菌被清除,而C-TiO₂和S-TiO₂组分别仅清除约13%和31%。SEM观察进一步证实,IrNC@TiO₂处理组生物膜完整性受到显著破坏。结晶紫染色定量分析表明,IrNC@TiO₂处理组在570 nm处的吸光度降幅最为显著,证实其具有优异的生物膜清除能力。这种高效的抗生物膜活性归因于酶催化产生的高浓度ROS与仿生尖刺表面结构的协同作用。分子动力学模拟采用由葡聚糖(EPS中常见组分)构建的简化生物膜模型, 对比了平面与尖刺TiO₂结构对生物膜的穿透行为。在20 ns模拟时间内,平面TiO₂在与生物膜表面接触后停滞不前,而尖刺TiO₂则持续向基质内部推进。相互作用能分析表明,尖刺结构穿透生物膜是一个能量有利的自发过程。综上,IrNC@TiO₂通过尖刺介导的物理穿透与ROS化学降解的双重机制,实现了对致密生物膜EPS基质的高效破坏与清除。
图5. IrNC@TiO₂抗变形链球菌生物膜性能评价。
VI 防龋性能评估
本研究在离体人牙模型上评估了IrNC@TiO₂的抗生物膜及防龋效果。 CLSM成像显示,对照组、H₂O₂组及C-TiO₂组牙齿表面形成典型的致龋生物膜,呈现密集的细菌簇包裹于EPS基质中。S-TiO₂组实现约26%的细菌杀灭,而IrNC@TiO₂组达到约74%的杀菌率,并伴随显著的EPS降解,表明其POD样活性不仅能杀灭细菌,还能通过自由基介导的催化作用破坏生物膜基质。SEM及Micro-CT观察表明, 对照组牙釉质表面出现严重的侵蚀和微空洞形成,而IrNC@TiO₂处理组牙釉质表面基本保持光滑完整,脱矿现象显著减少,牙本质小管暴露程度明显降低,证实IrNC@TiO₂能有效抑制生物膜酸介导的牙釉质脱矿。 IrNC@TiO₂作为日常或处方牙膏、漱口水的活性成分具有广阔前景。
图6. IrNC@TiO₂的龋病预防评估。
VII 总结
本研究提出了一种仿噬菌体人造酶材料(IrNC@TiO₂)的全新设计策略,在口腔生物膜清除与龋齿预防中实现了物理拓扑破膜与ROS催化杀菌的协同作用。
IrNC@TiO₂的海胆状尖刺拓扑结构模仿了噬菌体捕获细菌的尾丝机制,分子动力学模拟与电子显微镜证实其能够增强对细菌的机械捕获,并促进对细菌膜及胞外生物膜基质的穿透能力。 IrNC@TiO₂通过Ir–O配位将亚纳米Ir簇稳定锚定于TiO₂表面,形成驱动高效酶模拟活性的电子界面。密度泛函理论计算揭示了POD和HPO样ROS催化的有利反应路径,实现了口腔微环境中抗菌氧化物的持续、原位产生。抗菌效果上, 催化与物理的双重协同机制可有效清除变异链球菌,抑制牙齿表面生物膜成熟。在临床相关模型中,IrNC@TiO₂显著减少了牙釉质脱矿并预防了龋损形成。该材料在牙膏配方中表现出优于传统研磨剂的美白功效和去污能力,且未诱导出可检测的细胞毒性。从分子催化到宏观清洁的多功能性,使IrNC@TiO₂成为口腔卫生与治疗应用中有前景的平台。
这一仿生双引擎设计策略, 比起单纯优化酶活性或仅改善材料形貌的传统方法,更加集成、高效,尤其能助力高生物膜清除效率、低龋齿发生率的下一代口腔健康材料开发。本研究为设计兼具拓扑与催化活性的生物医用材料提供了可推广的策略,有望为其他生物膜相关感染性疾病的治疗开辟新路径。
作者简介

关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2024 JCR IF=36.3,学科排名Q1区前2%,中国科学院期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 四川大学程冲等: 一种仿噬菌体人造酶材料用于口腔生物膜高效抑制和龋病预防
 Nano-Micro Letters
Nano-Micro Letters 厦门大学楚成超/刘刚等综述:MOF纳米酶的精准设计、合成及生物医学应用
厦门大学楚成超/刘刚等综述:MOF纳米酶的精准设计、合成及生物医学应用 哈工大姜思达等:中熵双效催化剂探索“水-能”综合利用新策略
哈工大姜思达等:中熵双效催化剂探索“水-能”综合利用新策略 南航申来法团队:多价态化学驱动的高能水系锰电池储能体系
南航申来法团队:多价态化学驱动的高能水系锰电池储能体系 农环所申锋等:高熵催化剂如何“点木成金”,让生物质变高值化学品
农环所申锋等:高熵催化剂如何“点木成金”,让生物质变高值化学品