Metal-Organic Framework Nanozymes: From Rational Design and Synthesis to Biomedical Applications
Shundong Cai#, Mengdie Li#, Songyi Wang, Xiaofei Wen*, Gang Liu*, Chengchao Chu*
Nano-Micro Letters (2026)18:319
https://doi.org/10.1007/s40820-026-02168-x
本文亮点
1. 本综述讨论了金属离子和有机配体对MOF纳米酶催化活性的影响,为 MOF 纳米酶的理性设计提供了指导。
2. 本综述系统总结了 MOF 纳米酶在生物医学领域的最新研究进展。
3. 本综述详细讨论了MOF 纳米酶研究中目前面临的挑战并指明了未来的发展方向。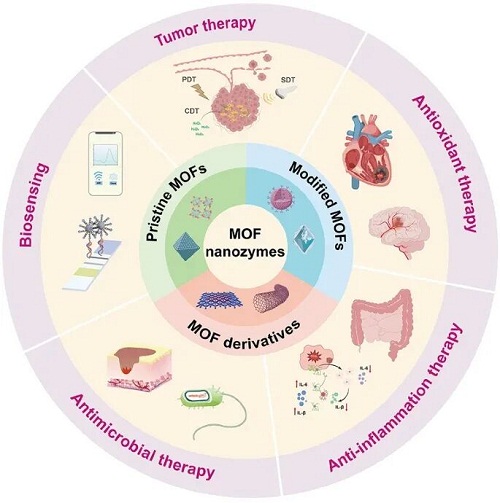
研究背景
近年来,金属有机框架(MOF)纳米酶在生物医学领域得到了广泛关注和研究。MOF 纳米酶的催化活性主要取决于金属离子与有机配体的配位环境。此外,对其形貌与孔径的精准调控也能显著提升催化效率。凭借其多种类酶活性,MOF 纳米酶在肿瘤治疗、抗炎和抗氧化治疗、抗菌、生物传感等方面展现出巨大的应用潜力。
内容简介
为了进一步推动MOF 纳米酶的理性设计,拓展其在生物医学领域的应用,厦门大学楚成超副教授、刘刚教授、温晓斐副研究员系统阐述了MOF纳米酶在生物医学领域的最新研究进展,并指明了未来发展方向。首先,本综述系统分析了金属离子、有机配体的选择以及形貌对MOF纳米酶催化活性的影响规律,并总结了不同合成方法的优缺点。其次,本文总结了MOF纳米酶具有的主要类酶活性,介绍了不同活性对应的应用领域和主要机理。接下来,通过具体的案例分析,本文介绍了 MOF 纳米酶在生物医学领域的主要应用及其潜在的催化机制。最后,本文深入剖析了MOF纳米酶在生物医学领域应用面临的关键挑战,并对未来的研究方向提出了展望。
图文导读
I MOF纳米酶在生物医学领域的研究得到快速发展
金属有机框架(MOFs)是由金属离子与有机配体通过配位作用形成的一类新型多孔材料,凭借其超高比表面积和可调控孔径,在催化、传感及药物递送领域展现出巨大优势。根据Web of Science数据库显示,到2025年,该领域的年发文量已超过250篇,反映出该研究领域取得了显著进展(图1)。相比于贵金属或碳基纳米酶,MOF纳米酶的核心优势体现在:首先,其结构高度可调,通过金属节点与配体的理性设计,可精准模拟天然酶活性中心或实现多金属协同催化。其次,丰富的孔道结构不仅提供了极高的活性位点密度,还能通过限域效应提升底物接触效率,并实现诊疗药物的集成负载。此外,MOF纳米酶合成工艺可控且稳定性优异,能在极端生理环境下保持活性。最后,其生物安全性具有可设计性,通过选用内源性配体及必需金属元素,可确保MOF纳米酶在体内降解为无毒副产物,显著降低了长期毒性风险。
图1. MOF纳米酶从2017年到2025年主要发展历程。
由于这些优越的性质,MOF纳米酶在生物医学领域得到了广泛研究,包括肿瘤治疗、氧化应激及炎症相关疾病治疗、抗菌治疗以及生物传感等。其核心功能主要通过调控活性氧(ROS)水平来实现。根据作用机制,MOF纳米酶可分为两大类:第一类是具有ROS清除活性的纳米酶(如类SOD、CAT、GPx),常通过中和病灶处过量的ROS来缓解氧化应激和炎症反应;第二类是具有ROS产生活性的纳米酶(如类OXD、POD),它们能在内源性或外源性刺激下产生大量有害ROS,从而实现对肿瘤细胞或病原菌的精准清除。此外,还有如类磷酸酶等非ROS调控型纳米酶,在有机磷农药检测等生物传感领域也展现出重要的应用价值。
II MOF纳米酶分类以及主要合成方法
如图2所示,根据其组成与结构,MOF纳米酶可分为原始MOF、改性MOF和MOF衍生物三大类。原始MOF指由金属离子与有机配体自组装形成的结晶多孔材料,直接利用其固有的金属中心或配体发挥类酶活性。其孔径分为微孔(< 2 nm)、介孔(2-50 nm)和大孔(> 50 nm),这种多孔结构为底物接触提供了充足的表面积和活性位点。改性MOF指通过配位键、共价键或物理吸附,在框架表面或孔隙中引入金属纳米颗粒(如Au、Pt)、功能配体或生物分子。这种策略在保持框架结构的同时,不仅能通过增强电子传输动力学来提升催化效率,还能赋予其靶向递送或控释等新功能。MOF衍生物指原始MOF经热解或化学转化后形成的金属氧化物/硫化物、金属-碳杂化材料或多孔碳材料。这些衍生物通常拥有极高的比表面积,展现出更强的类酶活性甚至多酶协同功能。
图2. MOF纳米酶的分类及代表性结构示意图。
III MOF纳米酶在肿瘤治疗中的应用
对于肿瘤,传统治疗手段(如手术、放化疗)虽然有效,但面临高复发率和严重副作用的挑战。与此同时,肿瘤微环境(TME)具有以下四大特征,为精准治疗提供了突破口:低氧、微酸性、高浓度过氧化氢以及显著升高的抗氧化物质。MOF 纳米酶在肿瘤治疗中展现出独特的“双重身份”,它能够原位催化产生高毒性的活性氧,直接破坏癌细胞。此外,MOF 的孔隙结构可负载药物,实现多种治疗模式的协同。同时,它还可以重塑免疫抑制性的肿瘤微环境。理性设计的 MOF 纳米酶系统通常集成了多种类酶活性。这些活性互为补充,在复杂的 TME 中各司其职,通过协同效应实现治疗效果的最大化。MOF 纳米酶通过产生 ROS 引发氧化损伤、程序性细胞死亡或微环境破坏。
基于MOF纳米酶的化学动力学疗法(CDT)核心依赖于过渡金属离子引发的类芬顿反应,通过将过氧化氢转化为高毒性的羟基自由基来杀伤癌细胞,而其效能的提升主要取决于多酶活性的级联协同:一方面,具备类SOD与类POD双重活性的纳米酶能将超氧阴离子级联转化为过氧化氢并最终生成羟基自由基,诱导细胞脂质过氧化;另一方面,集成类葡萄糖氧化酶活性可以通过消耗葡萄糖原位产生过氧化氢,为芬顿反应提供充足的化学底物,从而有效克服肿瘤微环境底物受限的问题,显著增强催化治疗的整体效果。此外,许多MOF纳米酶表现出类似过氧化氢酶(CAT)的活性,可应用于光动力治疗(PDT)和声动力疗法(SDT)。
IV MOF纳米酶在炎症和氧化应激相关疾病治疗中的应用
活性氧在生物体内具有双重作用:低浓度下作为信号分子调节细胞功能,而过度积累则会引发氧化应激与炎症的恶性循环,导致机体受损。因此,维持ROS产生与消除的平衡至关重要。具有类SOD、CAT及GPx等抗氧化酶活性的MOF纳米酶在治疗氧化应激与炎症相关疾病方面展现出巨大潜力。值得注意的是,通过在MOF系统中集成多种酶活性,可以模拟天然的完整酶促抗氧化通路,从而实现比单一功能材料更高效、更系统化的ROS清除。如图3所示,MOF 纳米酶在心脑血管疾病的治疗中展现出了多方面的疗效。它们能够实现靶向清除活性氧、调节炎症微环境,并促进组织修复。此外,MOF纳米酶可以应用于促进伤口愈合,主要作用机制是针对慢性创面中活性氧过量导致的持续炎症以及组织缺氧两大难题,并分解双氧水产生氧气以缓解创面缺氧状态。
图3. MOF纳米酶用于心脑血管疾病治疗。
V MOF纳米酶在抗菌治疗中的应用
对于抗生素耐药性这一全球性难题,MOF纳米酶凭借其多机制协同的杀菌模式展现出巨大应用潜力(图4)。其抗菌机制主要包括:通过类POD活性产生高毒性羟基自由基破坏细菌胞膜;释放金属离子干扰细菌代谢;利用类GPx活性耗尽细菌内的GSH以削弱其抗氧化防御系统;以及结合光热效应实现物理杀伤。相比传统抗生素,MOF纳米酶最核心的优势在于其通过物理破坏与化学攻击的协同作用,几乎不会诱发细菌产生耐药性,为治疗烧伤感染等临床难题提供了高效、持久的新型解决方案。
图4. MOF纳米酶用于抗菌治疗。
VI MOF纳米酶在生物传感中的应用
MOF纳米酶凭借其可调控的结构与催化活性,在生物传感领域展现出卓越的应用价值(图5)。其核心原理是利用纳米酶在目标分析物存在下诱发检测系统产生颜色、荧光或电化学等信号变化,且信号强度与目标物浓度呈定量关系。在实际应用中,基于比色法的传感平台因其显色直观、成本低廉及快速响应而备受青睐。荧光检测则以高灵敏度和多参数分辨率见长,而电化学传感通过将催化反应转化为电信号,实现了对复杂样本中痕量标志物及病原体的高灵敏、高特异性直接检测。这种多维度的检测手段为精准医疗和即时诊断提供了强有力的技术支撑。与传统材料相比,MOF纳米酶在生物传感领域具有显著的性能优势。首先,其高密度的活性位点分布与多孔结构产生的协同效应,大幅提升了电子传输效率,从而实现了更宽的线性范围和极低的检测限(LOD)。其次,MOF的结构高度可调,通过优化金属离子、配体或引入表面官能团,不仅能增强对目标物的催化活性与选择性,还能有效减少样本杂质的干扰。此外,其卓越的化学稳定性使其能在极端pH和温度环境下保持活性,且具备良好的重复利用性。
图5. MOF纳米酶用于生物传感。
VII MOF纳米酶研究面临的挑战和未来发展方向
虽然MOF纳米酶在生物医学领域展现出巨大潜力,但目前仍面临规模化生产困难、结构与性能关系尚未完全阐明、催化活性与特异性难以比拟天然酶,以及临床转化中的安全性与代谢风险等严峻挑战。为了解决这些挑战,未来的发展将聚焦于构建具备自组装与诊疗一体化能力的智能纳米机器人,并推动实验室传感平台向便携式商用检测设备的转化。同时,行业亟需建立标准化的催化活性评价体系,并深度整合AI技术贯穿从理性设计到自动化合成的全产业链,通过多学科交叉融合,最终实现MOF纳米酶在精准医疗中发挥更大的价值。
作者简介



关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2024 JCR IF=36.3,学科排名Q1区前2%,中国科学院期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 厦门大学楚成超/刘刚等综述:MOF纳米酶的精准设计、合成及生物医学应用
 Nano-Micro Letters
Nano-Micro Letters 四川大学程冲等: 一种仿噬菌体人造酶材料用于口腔生物膜高效抑制和龋病预防
四川大学程冲等: 一种仿噬菌体人造酶材料用于口腔生物膜高效抑制和龋病预防 哈工大姜思达等:中熵双效催化剂探索“水-能”综合利用新策略
哈工大姜思达等:中熵双效催化剂探索“水-能”综合利用新策略 南航申来法团队:多价态化学驱动的高能水系锰电池储能体系
南航申来法团队:多价态化学驱动的高能水系锰电池储能体系 农环所申锋等:高熵催化剂如何“点木成金”,让生物质变高值化学品
农环所申锋等:高熵催化剂如何“点木成金”,让生物质变高值化学品